-
不混溶两相的液-液界面合成技术是启动或改善化学反应的有效工具。在不混溶两相的合成中,亲水分子和疏水分子被限制在液-液界面发生反应。当界面环境改变时,反应动力学、反应产率和选择性也会得到改善[1],尤其是一些对水敏感的分子与亲水分子反应时,不混溶两相的液-液界面合成技术展现出巨大优势。如,对水敏感的疏水活性分子溶于有机相,亲水含氨基分子溶于水相,两相混合后,在液-液界面发生氨解形成酰胺键的反应[2]。活性酯在有机相中的水解受到抑制,酯氨解形成酰胺键的反应转化率得以提升。由于两相溶剂不混溶,确保亲水分子与疏水分子之间充分接触(即增加两相界面接触面积)的“媒介”显得尤为重要。使用磁力或机械搅拌器[3]、超声波辐照[4-6]和转子-定子均质机[7]等,在一定程度上能够增加不混溶两相间界面的接触面积,进而提高反应效率。然而,这些方法需与相转移催化剂结合使用,导致无法避免使用相转移催化剂带来的相关问题,例如热不稳定、成本高、产物难回收等[8]。因此,在无相转移催化剂的条件下,实现不混溶两相间疏水活性酯与亲水分子的高效氨解以形成酰胺键仍是一项巨大的挑战。
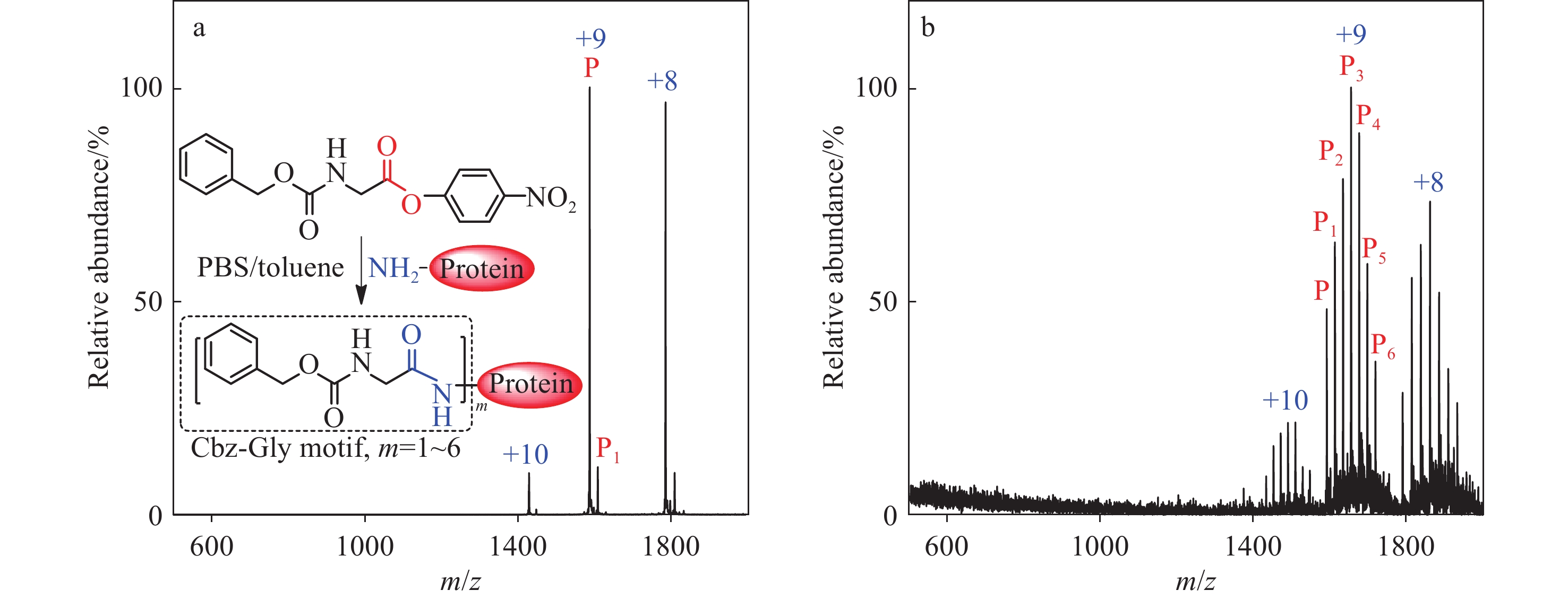
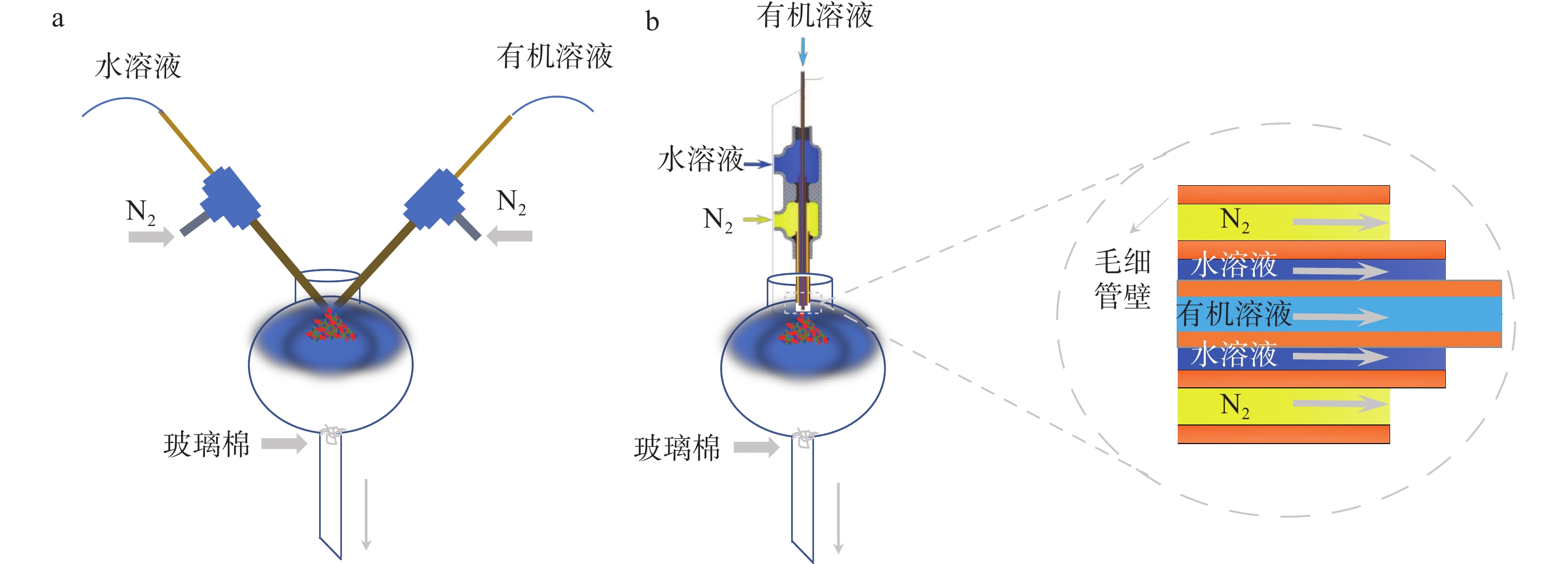
近几十年来,基于电喷雾质谱的微液滴化学已成为各种化学反应的便捷平台[9]。微液滴具有独特的物化性质,如反应物在微液滴-气体界面附近的部分溶剂化、微液滴的极端pH值、溶剂的快速蒸发及原料局部浓度提升、界面附近的特殊电场,以及增强的传质过程等[10]。近期,南开大学张新星研究员、杭州师范大学程和勇教授、斯坦福大学Zare教授、普渡大学Cooks教授、德州农工大学严昕教授等在微液滴化学性质方面的研究进展[11-15],进一步揭示了微液滴化学技术的重要作用。分子在液相和气相中反应速率的数量级差异,归因于反应分子的溶剂化[16]。作为部分溶剂化典型代表的微液滴体系,其反应过程的能垒显著低于本体溶液[17]。因此,微液滴中的反应可被加速至本体溶液的101~105倍,反应产率也能大幅提高[18-20]。2017年[21],严昕和Zare采用基于电喷雾萃取电离(EESI)原理的双液路非同轴微液滴技术(图1a),在无相转移催化剂的情况下,实现了不混溶两相中亲水的次氯酸钠氧化疏水的苄醇制备醛或酮(产率为50%~75%)。综上所述,微液滴化学技术在促进不混溶两相液-液界面反应、提高反应速率和产率等方面,展现出巨大潜力。
本文拟结合酯氨解形成酰胺键的特点和微液滴化学的技术优势,开发一种不混溶两相中亲水分子和疏水分子之间无需相转移催化剂的高效偶联方法。首先,以溶解于疏水溶剂中的活性酯与水溶液中蛋白氨解反应为模型,研究样品流速、鞘管压强、电场强度和有机溶剂对不混溶两相微液滴中酰胺键耦合效率的影响,探索无相转移催化剂条件下,微液滴技术促进不混溶体系中酰胺键偶联反应的基本规律。通过建立基于微液滴技术的不混溶两相中片段偶联的方法,实现无相转移催化剂时两相中亲水分子和疏水分子的高效偶联。
-
线性离子阱质谱仪:美国 Thermo Fisher Scientific 公司产品,配备 Xcalibur 程序;FA2204分析天平:上海良平仪器仪表有限公司产品;TG16.5台式高速离心机:上海卢湘仪离心机有限公司产品;PHS-3E型pH计:上海雷磁仪器有限公司产品;VM-T1涡轮混匀仪:上海泰坦科技有限公司产品;JetSpinTM-15超滤管:广州洁特生物过滤有限公司产品;LSP01-1Y恒流泵:融柏恒流泵有限公司产品;同轴三通道型电喷雾喷头:由江西省质谱科学与仪器重点实验室自制;实验用水(高纯水):由 7144型Thermo Scientific 纯水仪制备;高硼硅玻璃毛细管(1.2 mm×0.9 mm):美国世界精密仪器有限公司产品。
-
溶菌酶(~14 300 u):北京索莱宝科技有限公司产品;N-苄氧羰基-2-氨基乙酸对硝基苯酚酯(Z-Gly-ONP,纯度≥97%):安耐吉化学试剂有限公司产品;Na2HPO4·12H2O、NaH2PO4·2H2O、N,N-二甲基甲酰胺:均为分析纯,上海泰坦科技有限公司产品;甲醇、甲苯:均为色谱级,上海麦克林生化科技有限公司产品;乙酸乙酯、二氯甲烷、4-甲基-2-戊酮:均为分析纯,上海泰坦科技有限公司产品;仲丁醇、正丁醇:均为分析纯,安耐吉化学有限公司产品;熔融石英毛细管:美国安捷伦科技有限公司产品。
-
取27.2 mg溶菌酶于离心管中,加入3 mL 磷酸盐缓冲溶液(PBS,pH 7.4)使其溶解,得到0.6 mmol/L蛋白溶液。取29.7 mg Z-Gly-ONP于离心管中,加入3 mL有机溶剂使其溶解,得到30 mmol/L Z-Gly-ONP母液,再将该母液用对应有机溶剂稀释至6.0 mmol/L。用注射器分别吸取1 mL 0.6 mmol/L蛋白PBS溶液和1 mL 6.0 mmol/L Z-Gly-ONP有机溶液,将注射器针头通过管线及套管与三通喷头中2个液路相连,气路通道与氮气钢瓶相连,辅助液体雾化形成微液滴,进行微液滴反应。雾化液滴反应的出口与分液漏斗相连,用以收集微液滴反应产物,具体装置图示于图1。反应结束后,用15 mL甲醇-水-甲酸溶液(49.9:49.9:0.2,V/V/V)和30 mL水依次溶解漏斗中的产物,将所得的产物溶液进行超滤浓缩除盐和质谱鉴定。另将1 mL 0.6 mmol/L蛋白PBS溶液和1 mL 6.0 mmol/L Z-Gly-ONP有机溶液于5 mL反应瓶中直接混合,并在摇床混匀反应,以此作为溶液相反应参照。与微液滴相反应相同时间后,加入15 mL甲醇-水-甲酸溶液(49.9:49.9:0.2,V/V/V)终止反应,与微液滴反应产物进行相同的超滤、除盐、鉴定等操作。
在线性离子阱质谱仪上进行质谱测试,通过Xcalibur程序进行数据采集及分析,并使用拉针仪将高硼硅玻璃毛细管拉制成纳升电喷雾喷针。微液滴相和溶液相反应的相对转化率通过原料与产物的质谱信号相对强度计算得到[22-23],具体计算方法示于式(1)。其中,IPn为偶联上n个小分子的蛋白质谱信号强度(n=0,1,2,3······)。
-
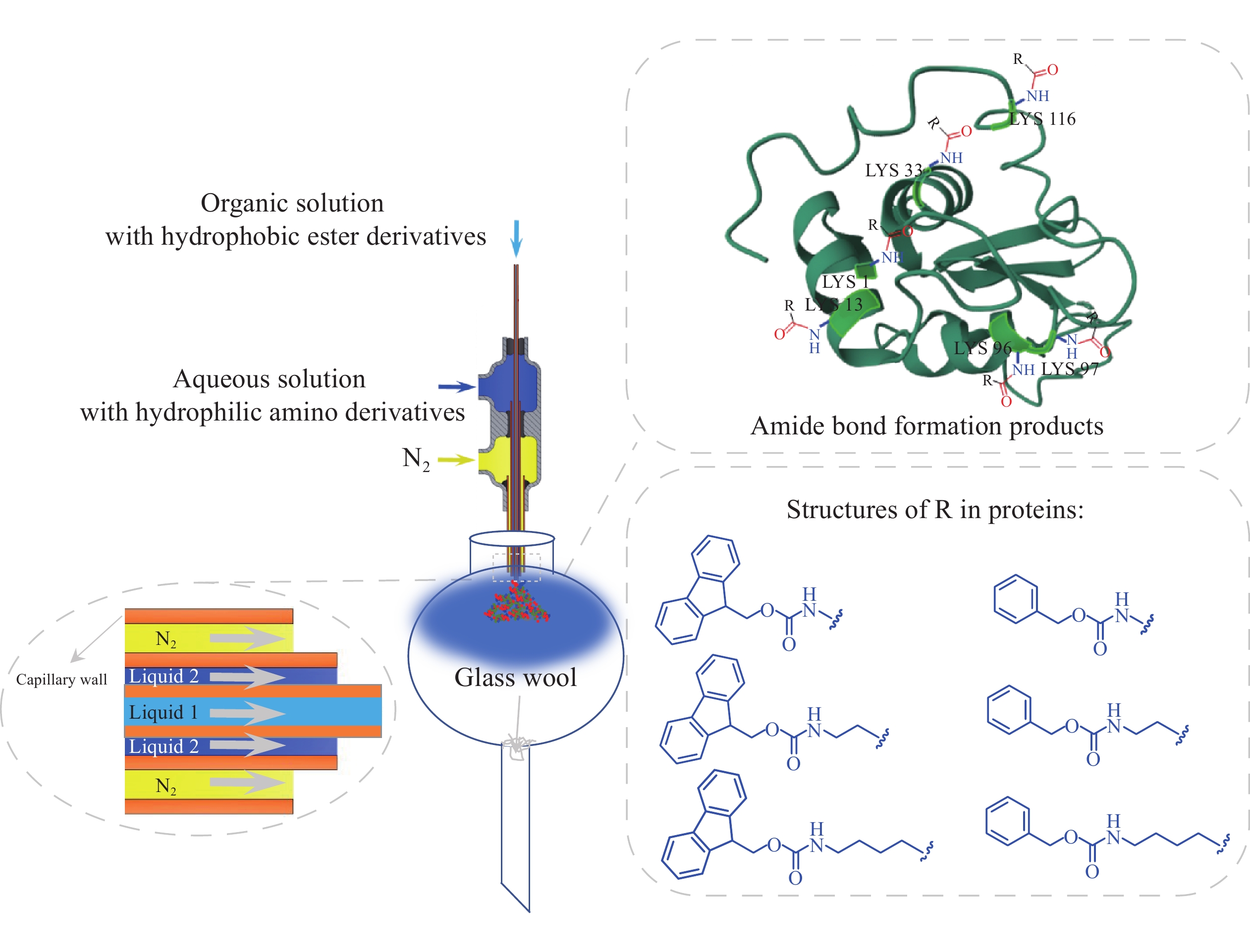
不混溶两相微液滴反应装置的核心是同轴三通道微液滴喷头,以及收集反应产物的样品接收瓶。喷头的2个液路通道与固定在注射泵的2个样品注射器相连,气体通道通过peek管和固定接头与高压氮气相连,用于辅助液体通道中的样品溶剂雾化形成微小液滴,装置示意图示于图1b。同轴三通道喷头的管路是由L1(0.1 mm×0.19 mm),L2(0.25 mm×0.35 mm),L3(0.45 mm×0.65 mm)3层规格不同的熔融石英毛细管同轴组成。L1和L2层套管分别流经样品溶液1和2,L3层套管流经氮气。由于3个管路是同轴套管形式组装,管路中的物质在管内经过时互不接触,只在微液滴喷口处的三维空间内(样品接收瓶的空间)接触并发生物质交换,通过氨解反应得到共价偶联产物。
将模型小分子酯(Z-Gly-ONP,Ea)的甲苯溶液和模型蛋白(溶菌酶P,~14 ku)的PBS溶液分别装入2个注射器中,含有Ea的甲苯溶液流经雾化喷头最内层管道(L1),蛋白PBS溶液流经中间管道(L2)。在PBS溶液的注射器针头处施加4.0 kV电压,雾化喷头的气路氮气钢瓶输出压强为0.8 MPa。在双通道注射泵推进下,两路液体缓慢地从雾化器喷口处流出,两路样品溶液在高速氮气的辅助下雾化成微小液滴,于喷口处三维空间内接触发生反应,用装有二氧化硅的分液漏斗收集喷雾。反应相同时间后,用甲醇-水-甲酸溶液(49.9:49.9:0.2,V/V/V)洗涤分液漏斗,然后将洗涤液超滤浓缩,浓缩液经稀释后,采用纳升电喷雾质谱(nano-electrospray ionization mass spectrometry,nESI-MS)鉴定。
质谱结果表明,本体溶液中的产物形成程度与微液滴中明显不同。在本体溶液中,收集到的产物在+8、+9、+10电荷处最大丰度质荷比分别为m/z 1 789(+8)、1 591(+9)、1 432(+10),其相对强度分别为97%、100%、11%,示于图2a。然而,m/z 1 789(+8)、1 591(+9)、1 432(+10)是模型蛋白原料P的信号。反应体系中仅发现Ea通过酰胺键与P偶联的产物P1(1个Ea与蛋白偶联的产物)。P1在+8、+9、+10电荷处的质荷比分别为m/z 1 813(+8)、1 612(+9)、1 451(+10),相对强度分别为12%、9%、<1%。根据相对反应转化率公式计算,常规溶液相中反应转化率为11%。结果表明,在常规溶液相反应中,反应物活性酯与P在相互溶解的溶液中发生酯胺解反应生成酰胺键产物的信号较低,导致偶联效率和相对转化率很低。
在微液滴反应中,模型蛋白P的信号强度相对较低,但可明显检测到6个Ea通过酰胺键与P偶联的产物(P1、P2、P3、P4、P5和P6),示于图2b。6个产物带+8~+10电荷的信号相对强度比分别为52%、66%、16%(P1),68%、80%、18%(P2),70%、100%、20%(P3),57%、89%、20%(P4),36%、57%、11%(P5),25%、33%、12%(P6),其中,微液滴反应系统的P1信号强度比(55:66:16)高于本体反应系统的P1信号强度比(12:9:<1)。此外,P2~P6在微液滴反应中表现出良好到优异的信号强度比,这是本体反应体系中没有的。根据相对反应转化率公式计算,微液滴相中反应转化率为96%。该结果表明,在微液滴反应系统中,活性酯和溶菌酶蛋白在不混溶两相中发生酯氨解形成酰胺键的反应转化效果良好。值得注意的是,在微液滴两相体系中,即使无相转移催化剂存在,2种不混溶的液体仍能接触并发生传质作用,使得活性酯与氨基反应形成酰胺键。这一现象可能主要归因于微液滴技术将溶液体系通过雾化器雾化成尺寸较小的液滴,使得两相间界面的接触面积增加多个数量级,有效改善了传质效果,进而能够更好地转化成相应的产物。
-
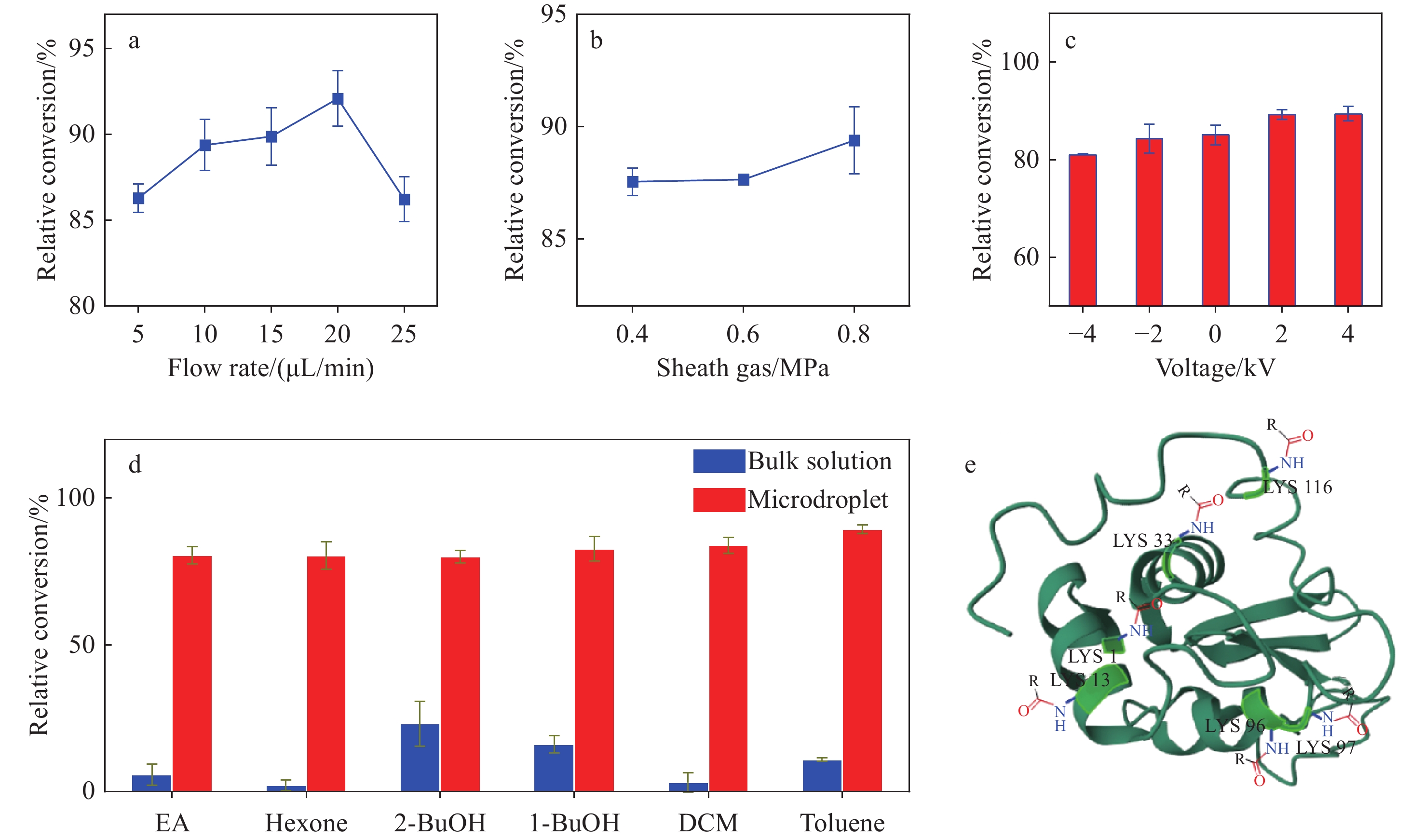
一般来说,影响微液滴反应的因素较多,如液体流速、鞘气压强、液体表面电荷、溶剂组成等。为深入了解无相转移催化剂条件下,不混溶两相微液滴中氨解构建酰胺键的效率,本实验进一步优化了微液滴反应条件,并通过相对转化率评估Ea和P的反应结果。当喷嘴中的液体流速增加时,微液滴的初始尺寸会增大。出乎意料的是,在不混溶两相微液滴体系中,当每个通道的流速从5 μL/min增至20 μL/min,且其他参数保持不变时,相对转化率从86%提升至92%,示于图3a。据文献报道[17],在一定流速范围(5~25 μL/min)内,随着液体流速降低,微液滴尺寸减小,相对转化率升高。但在不混溶两相微液滴中,随着液体流速降低,其相对转化率不一定会提高。不容忽视的是,在低流速(5 μL/min)和高压鞘气(0.8 MPa)的不混溶两相微液滴反应过程中,一些固体(起始反应物)易在喷嘴尖端积聚,这可能影响微液滴的飞行并抑制两相之间的传质。随着流速从20 μL/min增至25 μL/min,初始微液滴尺寸增大,表面积体积比降低,导致相对转化率从92%下降到86%。本实验还考察了鞘气压强对相对转化率的影响,示于图3b。当压强从0.4 MPa增至0.8 MPa时,相对转化率从88%提升至89%。这表明,在一定鞘气压强下,进一步增加鞘气压强对两相反应无显著影响。
实验还考察了喷雾电压在−4~4 kV范围内,不混溶两相微液滴间的反应,结果示于图3c。当不施加电压时,相对转化率仍达85%,这是由于高压(0.8 MPa)雾化气体的高速流动对喷嘴的初始液滴施加了强大的剪切应力,促使初始液滴变成更小的液滴。随着电压从0 kV上升到+2 kV,相对转化率逐渐从85%提升到88%。然而,当喷雾电压提高至+4 kV时,相对转化率约为88%,表明当喷雾电压达到一定值时,初始液滴尺寸不再进一步减小,相对转化率也不再进一步提高。当采用负电压时,相对转化率从84%下降到80%,这可能是因为在负离子条件下,生成的液滴表面可能易被阴离子(即HPO42−、H2PO4−或OH−)占据,而非阳离子(即Na+或H+加合的蛋白质),从而降低了蛋白质和酯之间界面的碰撞频率。此外,实验还开展了涉及多种疏水溶剂(如乙酸乙酯、己酮、二氯甲烷、正丁醇、甲苯)的离线带电微液滴反应,并将相应的相对转化率与本体反应进行比较,结果示于图3d。可见,在微液滴中氨解形成酰胺键的反应转化率良好,约为80%~91%,比本体溶液在不混溶体系中的氨解反应优势明显。
在常规溶液相中,蛋白的PBS溶剂与二氯甲烷、甲苯不互溶,反应分子仅在2个液相分层处界面有接触,分子间碰撞频率较低,反应不充分,导致溶液相中转化率较低。在微液滴中,2个不互溶液相之间的反应主要发生在液-液界面,微小液滴的液-液比表面积大,更有利于反应分子间的接触。因此,在不同的溶剂体系中,微液滴相较溶液相反应有明显优势。从优化条件可知,采用同轴三通道喷头进行微液滴反应时,当电压0 kV,雾化气体压强0.8 MPa,液体流速20 µL/min且溶解酯的溶剂为甲苯时,微液滴反应的转化率达到最优。
-
进一步探究了微液滴技术促进不混溶两相间酰胺键形成反应的底物适用范围,研究不同长度烷基链和不同大小疏水基团的疏水活性酯与溶菌酶两相间的氨解反应。不混溶两相中微液滴体系和溶液相体系反应的相对转化率,反应产物中最大偶联数,以及各产物对应离子的质荷比和相对强度列于表1。
从表1可知,在微液滴体系中,含有大疏水基团的活性酯类(Ea、Eb、Ec、Ed、Ee和Ef)可以有效地与P的氨基发生氨解反应,相对转化率为65%~91%,且得到的产物蛋白Pa、Pb、Pc、Pd、Pe和Pf(产物蛋白的核心结构示于图3e)均可检测到3~6个疏水基团与对应产物蛋白形成共价偶联。然而,在常规本体溶液体系中,Ea、Eb、Ec、Ed、Ee和Ef与蛋白P氨解共价偶联的相对转化率较低,均不超过11%。以带9个正电荷的蛋白质分子离子峰为例,相对离子强度≥30%的分子离子只有模型蛋白的离子峰m/z
1591 ,几乎未检测到疏水基团与P形成的Pa、Pb、Pc、Pd、Pe和Pf。由此可见,对于不混溶两相间氨解反应,微液滴体系的相对转化率显著高于常规溶液体系,且偶联效率差异悬殊(微液滴体系中模型蛋白上偶联的小分子个数为3~6个,而常规体系基本没有小分子发生偶联)。这可能是因为N-芴甲氧羰基(Fmoc基团)和N-苄氧羰基(Cbz基团)具有疏水性,在常规溶液相反应体系中,溶解小分子的有机溶剂(甲苯)与溶解蛋白的水溶液(PBS)之间出现明显分层现象。疏水的Fmoc和Cbz只能溶解在甲苯相中,两相体系分子较难接触反应,导致常规溶液相体系的相对转化率明显偏低。从表1中条目1~3数据可知,在微液滴反应中,当疏水基团为体积较小的Cbz时,反应的相对转化率分别为91%、86%、84%。实验发现,疏水基团与活性酯键之间烷基链最短的Ea小分子相对转化率最高,这可能是因为烷基链越短(氨基甲酸酯基团与酯键基团间只有1个亚甲基),吸电子的氨基甲酸酯基团对酯键的影响越显著,导致活性酯中羰基更不稳定,更易与氨基发生氨解反应形成酰胺键,导致转化率升高。当烷基链长度增加(氨基甲酸酯基团与酯键基团间有3~5个亚甲基)时,吸电子的氨基甲酸酯基团对酯键的影响明显减弱,Eb和Ec小分子的相对转化率明显低于Ea。从条目4~6可知,当疏水基团为体积较大的Fmoc时,Ed、Ee和Ef与P在不混溶两相微液滴中反应的相对转化率分别为65%、67%、72%。综合条目1~6可知,含有Fmoc基团活性酯的转化率显著低于Cbz基团活性酯,这可能是因为Fmoc体积较大且具有较大的共轭体系,会分散氨基甲酸酯基团周围的电子云密度,降低其电负性和吸电子能力,导致氨基甲酸酯基团对活性酯基团的吸电子能力减弱,使其与氨基发生氨解反应形成酰胺键的能力下降,最终使相对转化率降低。
-
针对无相转移催化剂时不混溶两相间酰胺键构建过程中的瓶颈问题,利用微液滴化学技术优势,设计组装了可促进不混溶两相间液-液界面充分接触的微液滴反应装置,实现了两相间物质的共价偶联及产物收集,并结合质谱技术,快速监测分析微液滴中不混溶两相间反应。以疏水小分子酯与亲水多肽的氨基氨解形成酰胺键的反应作为微液滴中不混溶两相间反应的模型,阐明微液滴中传质方式、微液滴尺寸、电场强度、溶剂极性等因素对不混溶两相间界面的影响,成功实现了无相转移催化剂时两相中亲水分子与疏水分子的高效偶联,为不混溶两相中亲水蛋白与疏水分子间无需相转移催化剂的高效偶联提供了新方法。
微液滴技术促进不混溶两相间酰胺键形成反应的质谱研究
Microdroplet-promoted Amide Bond Formation between Substances on the Interface of Two Immiscible Liquid Phases
-
摘要: 不混溶两相中酰胺键的形成对不同亲疏水官能团间的共价偶联具有重要意义。本文采用同轴双液路喷雾装置,探索微液滴技术在促进不混溶两相间物质氨解反应形成酰胺键的优势。首先,以N-苄氧羰基-2-氨基乙酸对硝基苯酚酯(Ea)与溶菌酶蛋白氨解反应为模型,研究样品流速、鞘管压强和溶剂等因素对不混溶两相微液滴中氨解效率的影响。研究发现,样品流速和鞘管压强对反应效率起到关键作用,可能是由于高压气流对流速较低的初始液滴施加强大的剪切应力,促使初始液滴变小,进而提高两相间物质交换效率。当氨解反应分别采用几种疏水性有机溶剂(如甲苯、乙酸乙酯、己酮、二氯甲烷、正丁醇)时,微液滴中的相对转化率在80%~91%之间。当小分子是带有大疏水基团的活性酯类Ea、Eb(N-苄氧羰基-4-氨基乙酸对硝基苯酚酯)、Ec(N-苄氧羰基-6-氨基乙酸对硝基苯酚酯)、Ed(N-芴甲氧羰基-2-氨基乙酸对硝基苯酚酯)、Ee(N-芴甲氧羰基-4-氨基乙酸对硝基苯酚酯)和Ef(N-芴甲氧羰基-6-氨基乙酸对硝基苯酚酯)时,微液滴体系中的氨解相对转化率在65%~91%之间,而在本体溶液中的相对转化率小于11%。由此可见,微液滴中不混溶两相间的氨解反应具有较广的底物适用范围,该方法在不同亲疏水官能团的共价偶联方面展现出潜在的应用价值。Abstract: Effectively constructing amide bonds between substances on the interface of two immiscible solvents plays a key role in the covalent-conjugation of the two substances with totally different hydrophilicity. In this study, a coaxial dual-channel spraying device was used to explore the advantages of microdroplet techniques in promoting the aminolysis between substances at the interface of two immiscible solvents for amide bond formation. The effects of sample flow rate, sheath pressure, electric field strength and organic solvent on the coupling efficiency of amide bonds in two immiscible microdroplets were studied, using Z-glycine-4-nitrophenyl ester (Ea) dissolved in an organic solvent and lysozyme protein (P) dissolved in an aqueous buffer as model substrates. When the sheath pressure was 0.8 MPa, as the flow rate increased from 5 μL/min to 25 μL/min, and the conversion increased first and then decreased from 92% to 86%. This may be due to the fact that under the conditions of low flow rate (5 μL/min) and high pressure of sheath gas (0.8 MPa), solids tend to accumulate at the nozzle tip, affecting the flight of microdroplets and suppressing mass transfer between two immiscible phases. When the flow rate was too high, the initial droplet was too large, leading to a reducation in the liquid-liquid specific surface area and a decrease in relative conversion (R.C.). When the flow rate was 10 μL/min, pressure of the sheath increased ranging from 0.4 MPa to 0.8 MPa or the voltage changing from 0 kV to ±4 kV, and all R. C. were ≥85%. It was proposed that the high-pressure gas flow (≥0.4 MPa) plays a major role by exerting strong shear stress on the initial droplet, promoting the conversion of initial large droplets to smaller ones to increase the surface-to-volume ratio of the liquid-liquid interface and enhance the mass exchange efficiency between the two phases. When several hydrophobic organic solvents (such as toluene, ethyl acetate, hexanone, dichloromethane, n-butanol) were used in the two-phased aminolysis reaction, the conversion rates in the microdroplets system are 80%-91%, and the highest conversion rate is 91% in toluene. However, the ammonolysis reaction in the bulk solution shows obvious lower conversion rate (≤21%). Finally, when the activated esters were Ea, Eb (N-benzoxycarbonyl 4-amino-acetic acid p-nitrophenol ester), Ec (N-benzoxycarbonyl 6-amino-acetic acid p-nitrophenol ester), Ed (N-fluorenyl methoxycarbonyl 2-amino-acetic acid p-nitrophenol ester), Ee (N-fluorenyl methoxycarbonyl 4-amino-acetic acid p-nitrophenol ester), or Ef (N-fluorenyl methoxycarbonyl 6-amino-acetic acid p-nitrophenol ester) with large hydrophobic groups, the R.C. of the aminolysis reaction in the two immiscible droplet systems is 65%-91%, while corresponding R.C. in the bulk solution is less than 11%, which is much lower than that in the microdroplets systems, indicating that microdroplet technique has applicable to a wide range of substrates for promoting the amide bonds construction between substances at the interfaces of two liquid phases. This strategy opens an avenue of microdroplets technique in the covalent coupling of functional groups with different hydrophilicity.
-
Key words:
- microdroplets /
- amide bond formation /
- two-phased reaction /
- mass spectrometry .
-

-
图 3 不混溶两相微液滴体系中Ea与模型蛋白P氨解反应的溶液流速(a)、雾化气体压强(b)、电压(c)和溶剂种类条件(d)的优化,以及产物蛋白结构图(e)
Figure 3. Optimization of reaction parameters including flow rate (a), carrier gas pressure (b), discharged voltage (c) and solvents (d) for microdroplet reaction between activated ester Ea and model protein P, and general structure for the product proteins (e)
表 1 不混溶两相中不同结构特点的活性酯与蛋白氨解反应效率
Table 1. Aminolysis of various ester substrates with protein in two-phased microdroplets
序号No. R基团结构
Structure of R group反应相对转化率
(反应产物中最大偶联数) R.C. (n)相对强度比≥30%的离子(带9个正电荷),
括号中为离子相对强度(%)
Ions with intensity ratio ≥30% (with 9 positive charges),
the value of ions intensity ratio (%) in parentheses微液滴体系
Microdroplet
system溶液相体系
Bulk solution
system微液滴体系
Microdroplet
system溶液相体系
Bulk solution
system1 
91(6) 11(0) 1591 (46),1612 (66),1633 (80),1654 (100),1676 (89),1697 (57),1718 (33) 1591 (97) 2 
86(5) <5(0) 1591 (69),1615 (90),1639 (98),1663 (88),1688 (61),1712 (32) 1591 (100) 3 
84(5) <5(0) 1591 (83),1618 (92),1645 (100),1672 (98),1700 (73),1728 (43) 1591 (100) 4 
65(3) 9(0) 1591 (77),1622 (50),1653 (42),1684 (30) 1591 (76) 5 
67(3) <5(0) 1591 (100),1625 (82),1659 (58),1693 (33) 1591 (100) 6 
72(3) <5(0) 1591 (66),1628 (72),1665 (55),1702 (31) 1591 (78) -
[1] PIRADASHVILI K, ALEXANDRIN O E M, WURM F R, LANDFESTER K. Reactions and polymerizations at the liquid-liquid interface[J]. Chemical Reviews, 2016, 116(4): 2 141-2 169. [2] CAROTHERS W H. Linear polyamides and their production: US, US2130523A[P]. 1938-09-20. [3] STARKS C M, LIOTTA C L, HALPERN M E. Phase-transfer catalysis: fundamentals I[M]//Phase-Transfer Catalysis. Dordrecht: Springer Netherlands, 1994: 23-47. [4] ABIMANNAN P, SELVARAJ V, RAJENDRAN V. Sonication effect on the reaction of 4-bromo-1-methylbenzene with sodium sulfide in liquid-liquid multi-site phase-transfer catalysis condition-kinetic study[J]. Ultrasonics Sonochemistry, 2015, 23: 156 -164 . doi: 10.1016/j.ultsonch.2014.08.006[5] SIVAMANI J, ASHOKKUMAR V, SADHASIVAM V, DURAIMURUGAN K, SIVA A. Ultrasonic assisted dimeric cinchona based chiral phase transfer catalysts for highly enanatioselective synthesis of epoxidation of α,β-unsaturated ketones[J]. RSC Advance, 2014, 4(104): 60 293-60 299. [6] EZQUERRA J, ALVAREZ-BUILLA J. Phase transfer catalysis under ultrasound. Alkylation of isoquinoline Reissert compound[J]. Journal of the Chemical Society, Chemical Communications, 1984(1): 54 . doi: 10.1039/c39840000054[7] KANO T, AOTA Y, MARUOKA K. Rate acceleration of solid-liquid phase-transfer catalysis by rotor-stator homogenizer[J]. Advanced Synthesis & Catalysis, 2016, 358(18): 2 996-2 999. [8] MICHAŁ F, MAGDALENA J Z, BARBARA K. Phase transfer catalysis in pharmaceutical industry-where are we?[J]. Acta Poloniae Pharmaceutica, 2008, 65(6): 647 -654 .[9] WEI Z, LI Y, COOKS R G, YAN X. Accelerated reaction kinetics in microdroplets: overview and recent developments[J]. Annual Review of Physical Chemistry, 2020, 71(1): 31 -51 . doi: 10.1146/annurev-physchem-121319-110654[10] DU J J, WANG C W, XU W B, ZHANG L, TANG Y K, ZHOU S H, GAO X F, YANG G F, GUO J. Multifunctional protein conjugates with built-in adjuvant (adjuvant-protein-antigen) as cancer vaccines boost potent immune responses[J]. iScience, 2020, 23(3): 100 935. [11] XUE L, ZHENG B, SUN J, LIU J, CHENG H. Water microdroplet chemistry for accelerating green thiocyanation and discovering water-controlled divergence[J]. ACS Sustainable Chemistry & Engineering, 2023, 11(34): 12 780-12 789. [12] SONG X, MENG Y, ZARE R N. Spraying water microdroplets containing 1,2,3-triazole converts carbon dioxide into formic acid[J]. Journal of the American Chemical Society, 2022, 144(37): 16 744-16 748. [13] ZHU C, PHAM L N, YUAN X, OUYANG H, COOTE M L, ZHANG X. High electric fields on water microdroplets catalyze spontaneous and fast reactions in halogen-bond complexes[J]. Journal of the American Chemical Society, 2023, 145(39): 21 207-21 212. [14] WANG T, LI Z, GAO H, HU J, CHEN H Y, XU J J. Ultrafast C–C and C–N bond formation reactions in water microdroplets facilitated by the spontaneous generation of carbocations[J]. Chemical Science, 2023, 14(41): 11 515-11 520. [15] LI M, BOOTHBY C, CONTINETTI R E, GRASSIAN V H. Size-dependent sigmoidal reaction kinetics for pyruvic acid condensation at the air-water interface in aqueous microdroplets[J]. Journal of the American Chemical Society, 2023, 145(41): 22 317-22 321. [16] CHABINYC M L, CRAIG S L, REGAN C K, BRAUMAN J I. Gas-phase ionic reactions: dynamics and mechanism of nucleophilic displacements[J]. Science, 1998, 279(5 358): 1 882-1 886. [17] YAN X, BAIN R M, COOKS R G. Organic reactions in microdroplets: reaction acceleration revealed by mass spectrometry[J]. Angewandte Chemie International Edition, 2016, 55(42): 12 960-12 972. [18] MÜLLER T, BADU-TAWIAH A, COOKS R G. Accelerated carbon-carbon bond-forming reactions in preparative electrospray[J]. Angewandte Chemie International Edition, 2012, 51(47): 11 832-11 835. [19] SAHOTA N, AbuSALIM D I, WANG M, BROWN C J, ZHANG Z, EL-BABA T J, COOK S P, CLEMMER D E. A microdroplet-accelerated Biginelli reaction: mechanisms and separation of isomers using IMS-MS[J]. Chemical Science, 2019, 10(18): 4 822-4 827. [20] YAN X. Emerging microdroplet chemistry for synthesis and analysis[J]. International Journal of Mass Spectrometry, 2021, 468: 116 639. [21] YAN X, CHENG H, ZARE R N. Two-phase reactions in microdroplets without the use of phase-transfer catalysts[J]. Angewandte Chemie International Edition, 2017, 56(13): 3 562-3 565. [22] GAO D, JIN F, LEE J K, ZARE R N. Aqueous microdroplets containing only ketones or aldehydes undergo Dakin and Baeyer-Villiger reactions[J]. Chemical Science, 2019, 10(48): 10 974-10 978. [23] GAO X F, CHENG J C, YE C L, XIAO S, QIU Z M, ZHANG X. Water promoted 9-fluorenylmethyloxycarbonyl detachment from amino acids in charged microdroplets[J]. Organic & Biomolecular Chemistry, 2022, 20(35): 7 001-7 005. -


 首页
首页 登录
登录 注册
注册


 下载:
下载: