-
化橘红,又称化州柚,是茂名化州市的道地中药材,广东省“十大珍稀中药材”品种之一,已有1 500多年的种植历史,因化痰奇效而得到国内外医学家的认可,有“南方人参”和“一片值一金”的美誉,且在化州的产量和功效远高于其他地区[1]。与取材于橘的橘红不同,化橘红取材于芸香科植物化州柚(Citrus grandis ‘Tomentosa’)或柚(Citrus grandis (L.) Osbeck)[2]未成熟或近成熟的干燥外层果皮,人们习惯将“化橘红”中药材及其原料植物统称为化橘红。目前,药材市场上的化橘红种类繁多,不同产地间的组分差异较大,因此,开展化橘红产地鉴别并找出特征标志物具有重要意义。
橘红中主要的有效成分为挥发油、黄酮、香豆素类化合物和多糖[3],各产地的成分含量不同。芦海生等[4]采用DNA条码技术和超高效液相色谱(UPLC)对2个不同产地的橘红进行区分;高泽林等[5]采用高效液相色谱(HPLC)测定不同基原、不同规格化橘红中柚皮苷、野漆树苷的含量,得出了不同化橘红之间的差异。为了比较广西引种栽培与道地产区广东化州化橘红的成分差异,王晓峰等[6]采用水蒸气蒸馏法和液相色谱-质谱(LC-MS)法分别测定广西陆川县、百色市、南宁市、广东化州市种植的橘红中挥发油成分,分析得出道地产地化州与陆川、南宁的共有成分差异较小,而与百色相差较大;周伟明等[7]采用固相微萃取-气相色谱-质谱联用技术检测和区分毛橘红和光橘红的挥发性物质,还采用近红外光谱技术对不经任何化学处理的原始样品(毛橘红、光橘红、伪品)进行直接检测,通过聚类分析法和主成分分析法对样品进行定性分析,实现了化橘红的快速无损鉴别[8]。
目前常用的中药鉴别方法中,UPLC和DNA条码技术通常需要复杂的前处理过程,耗时较长;近红外光谱技术的测试灵敏度较低,相对误差较大;GC-MS在分析复杂体系样品时存在基质干扰大及共流出严重等问题。
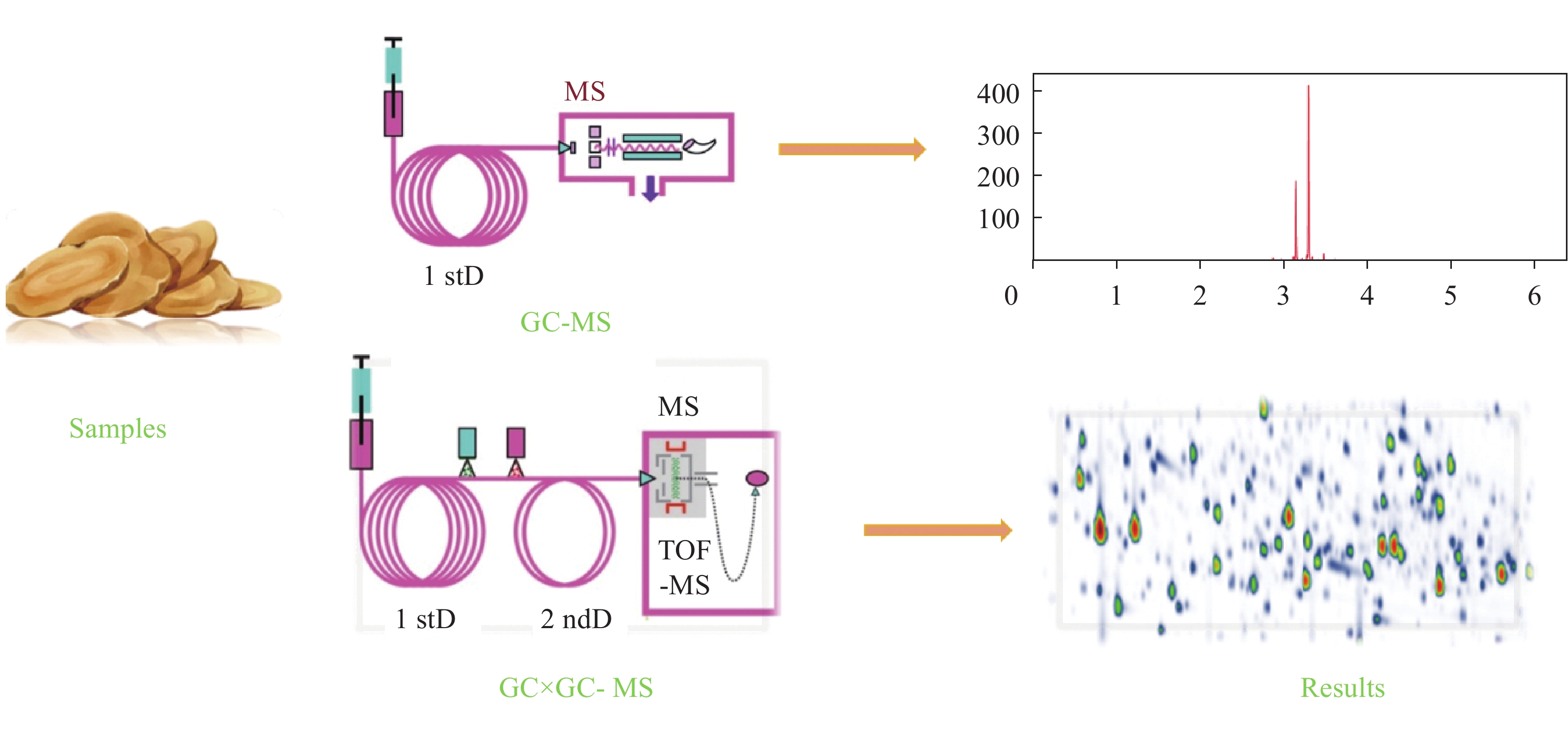
全二维气相色谱-飞行时间质谱(GC×GC-TOF MS)具有峰容量大、分离能力强、灵敏度高、定性准确等优点[9];便携GC-MS具有检测速度快的优点。鉴于此,本研究拟采用便携GC-MS和GC×GC-TOF MS分析化州橘红和广西橘红,找出两者之间的差异物质,以实现有效鉴别。
-
便携式GC-MS2000搭配便携式顶空进样装置(HSP1000)、GGT0620全二维气相色谱-质谱联用仪:广州禾信仪器股份有限公司产品;CTC RTC1200全自动多功能在线前处理进样器:瑞士CTC公司产品; Arrow 1.10 mm DVB/Carbon WR/PDMS固相微萃取头(膜厚120 μm):广州智达实验室科技有限公司产品;高速粉碎机:浙江屹立工贸有限公司产品。
-
橘红样品:由国药集团冯了性(佛山)药业有限公司提供,分别来自广东省茂名市化州市(CGEH)和广西省(CGEG),每种样品6个批次,共12个。将0.5 g经粉碎机粉碎的橘红药材放入20 mL顶空瓶中,密封保存。
-
色谱条件:DB-5色谱柱(6 m×0.1 mm×0.4 µm);进样口温度250 ℃,解吸温度250 ℃;分流比50∶1;载气(氦气)流速0.2 mL/min;程序升温:初始温度50 ℃,保持1 min,以35 ℃/min升至120 ℃,再以120 ℃/min升至260 ℃,保持2.5 min;顶空进样方式,采样1 min,预解吸0.5 min,解吸进样0.5 min,热吹扫2 min,分离4.17 min。
质谱条件:电子轰击(EI)源,离子源温度200 ℃,接口温度250 ℃,检测器电压−1 250 V,采集范围m/z 40~400。
-
气相色谱条件:进样温度240 ℃;分流比30∶1;DB-WAX一维色谱柱(60 m×0.25 mm×0.25 μm),DB-17MS二维色谱柱(2.3 m×0.18 mm×0.18 μm);载气为氦气;柱流量1 mL/min;程序升温:起始温度40 ℃,保持1 min,以3 ℃/min升温至241 ℃,保持10 min。
调制器条件:采用固态热调制器,选择HV调制柱(1.3 m×0.25 μm),调制周期6 s。
飞行时间质谱条件:EI源,电离能量70 eV,灯丝发射电流200 μA,离子源温度230 ℃,接口温度250 ℃,倍增器电压−1 850 V,采集范围m/z 50~500,采集速率100谱/s。
-
便携GC-MS数据:采用GC-MS处理软件(广州禾信,V1.0)通过对每个化合物的质谱图进行NIST17谱库比对检索以实现定性鉴定;GC×GC-TOF MS数据:采用全二维数据处理工作站软件Canvas(雪景科技,V2.5.0)对信噪比大于20的峰自动识别,通过对每个化合物的质谱图进行NIST17谱库比对检索以实现定性鉴定,其中选择正、反匹配度均大于800的化合物;采用C7~C30正构烷烃标准溶液(1 mg/L)进行保留指数(retention index,RI)测定。
-
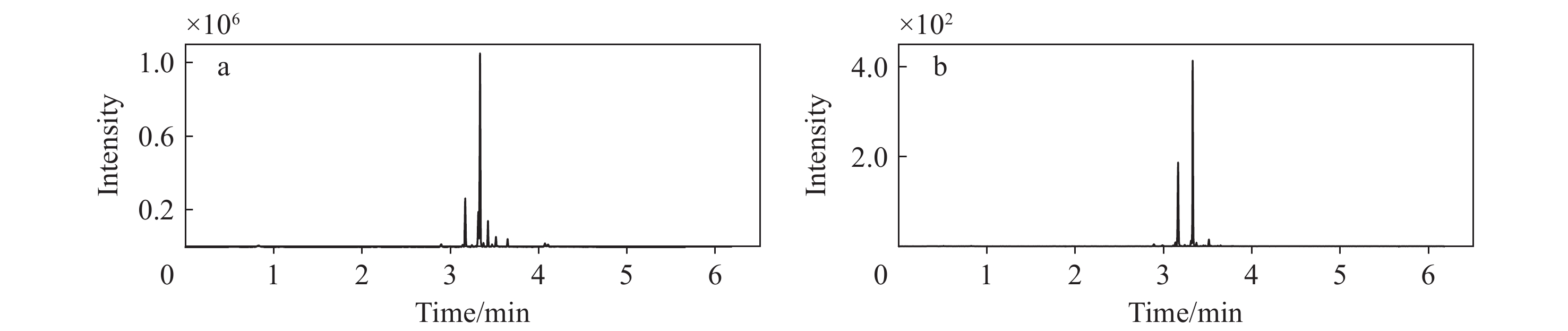
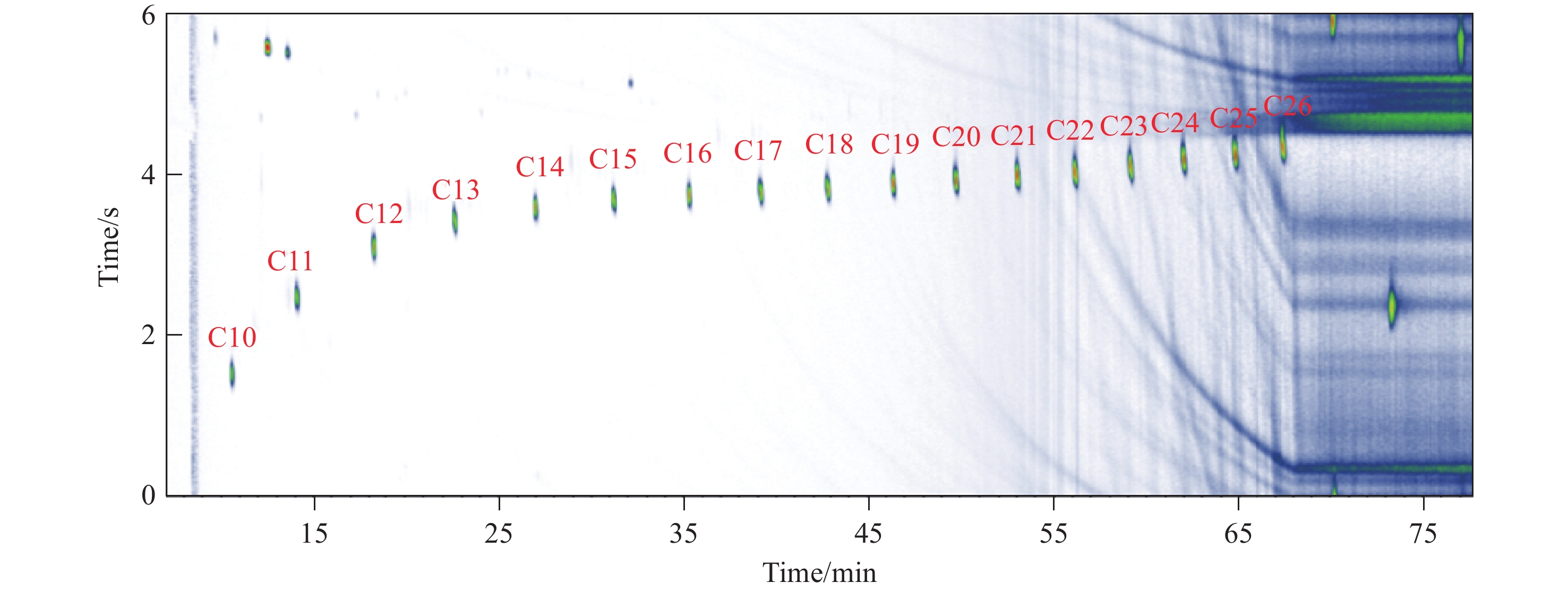
为获得RI并表征仪器系统的状况,采用液体进样方式将1 μL C7~C30正构烷烃标准溶液注入进样口中,按照1.3.2节条件操作,结果示于图1和表1。
-
本实验采用便携GC-MS对2个产地的橘红样品进行检测,发现谱图基本一致,示于图2。从谱图可见,化州橘红中检出的化合物较多,且2种橘红的最高峰均在3.1 min左右,为柠檬烯,但在化州橘红中的响应强度明显高于广西橘红,推断化州橘红的柠檬烯含量较高;4 min后,在化州橘红中还检出檀香醇,而广西橘红中无物质检出。通过对数据进行定性分析,罗勒烯、3-蒈烯、β-蒎烯、2,5-十八碳二炔酸甲酯、檀香醇这5种物质只在化州橘红中检出,可作为区分化州橘红与广西橘红的差异化合物,列于表2。
-
本实验采用GC×GC-TOF MS检测到化州橘红中223种挥发性物质,其中烯烃类含量最高,占比为25.56%~47.55%(6批次样品的平均含量为43.09%),醇类占比为16.05%~27.96%(平均含量为19.04%),芳烃类占比为15.44%~19.27%(平均含量为18.19%);在广西橘红中检测出252种物质,烯烃类含量最高,占比为43.07%~45.62%(平均含量为44.4%),芳烃类占比为21.44%~22.49%(平均含量为22.1%),醇类占比为11.65%~12.68%(平均含量为12.25%)。
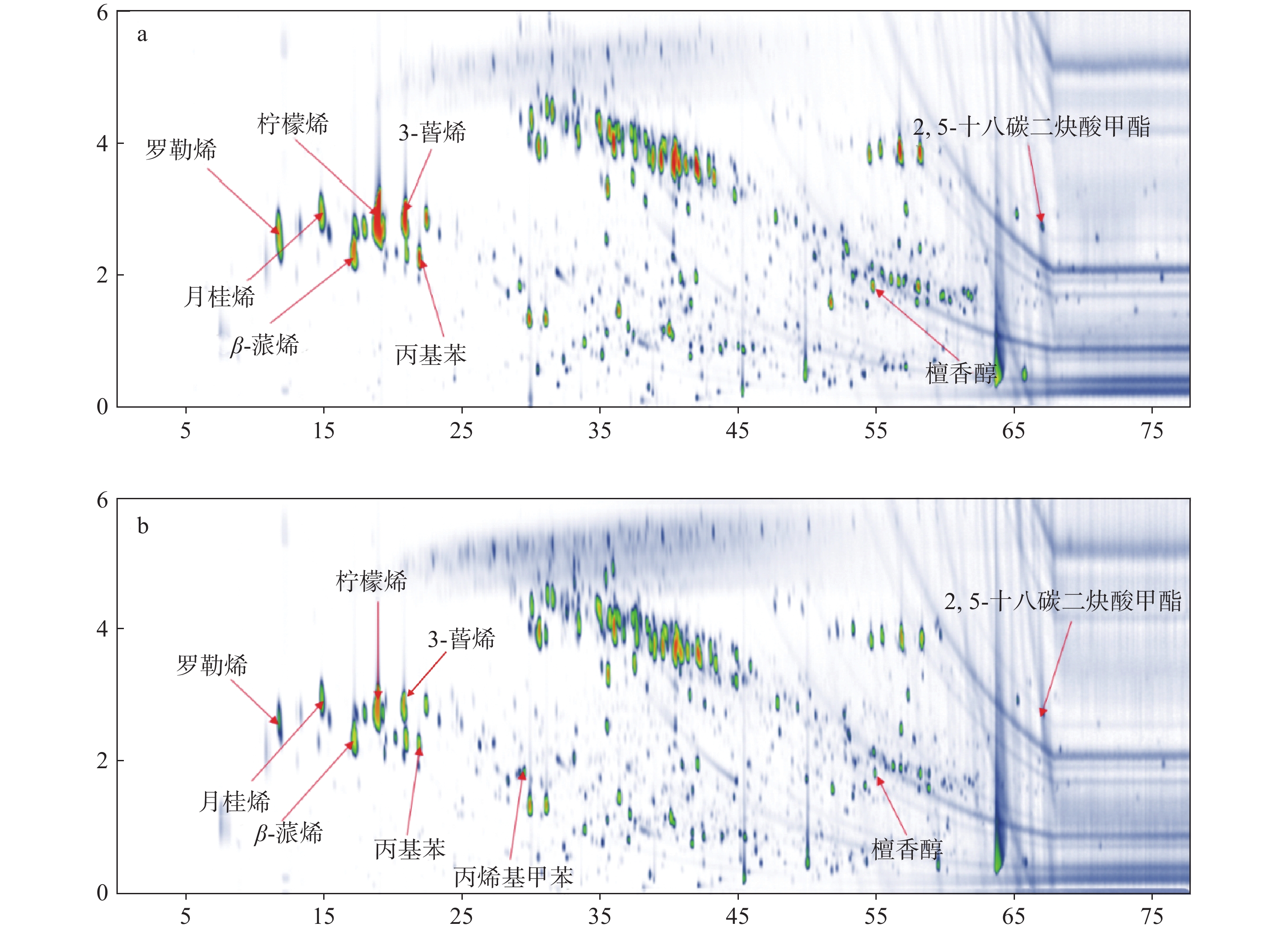
化州橘红和广西橘红的GC×GC-TOF MS色谱图示于图3。可见,2种橘红中的化合物种类差异较小,主要成分均为烯烃类物质,这与便携GC-MS的分析结果一致。另外发现,广西橘红同样含有罗勒烯、3-蒈烯、β-蒎烯、2,5-十八碳二炔酸甲酯、檀香醇这5种物质,但响应强度低于化州橘红,这与便携GC-MS结果不一致,表明便携GC-MS只能实现对2个产地橘红的初步鉴别。
进一步对GC×GC-TOF MS结果进行分析,化州橘红和广西橘红中的物质种类差别较小,但化州橘红的部分成分含量较广西橘红高,如柠檬烯、α-蒎烯、石竹烯;2种橘红中柠檬烯、β-蒎烯、石竹烯、γ-松油烯、γ-杜松烯的含量均较高。其中,化州橘红和广西橘红中柠檬烯的平均含量分别为8.58%、5.64%,柠檬烯具有平喘、镇咳、抗变性炎症和化痰之功效[11],临床上用于治疗胆囊炎[12],由此可以推测,化州橘红的止咳化痰效果好于广西橘红的可能原因是柠檬烯含量不同。γ-杜松烯具有抗菌、杀菌、祛痰的作用[13],是橘红止咳化痰的功效成分,2种橘红中的γ-杜松烯含量均为3.3%左右;α-蒎烯也具有明显的镇咳和祛痰作用[11];石竹烯有活泼猛烈的丁香气味,具有消炎[14]、止痛、麻痹、暖身、缓解胃炎等作用,对橘红止咳化痰功效起到了一定的作用,另外,还具有对皮肤和组织的抚慰功效[15]。广西橘红中含有2,3,5-三甲基吡嗪,其是一种高档香料,具有浓郁的烤花生或马铃薯香气,常用作结核、抗惊厥药物和抗菌剂[16],对止咳化痰作用较小。
-
化学计量学用于优化化学测量过程,并最大限度地从化学测量数据中提取有用信息[17-18]。主成分分析(PCA)是一种无监督的多元统计方法,可以在最大程度保留数据原始信息的基础上区分样本[19],是一种常用且有效的信息压缩方法,可将大量信息(变量)压缩为几个新的虚拟变量以简化问题。正交偏最小二乘判别分析(OPLS-DA)是一种有监督的多元统计方法,可提取有利于样本分类的变量信息,减少系统噪声干扰,提高分类效率[20]。
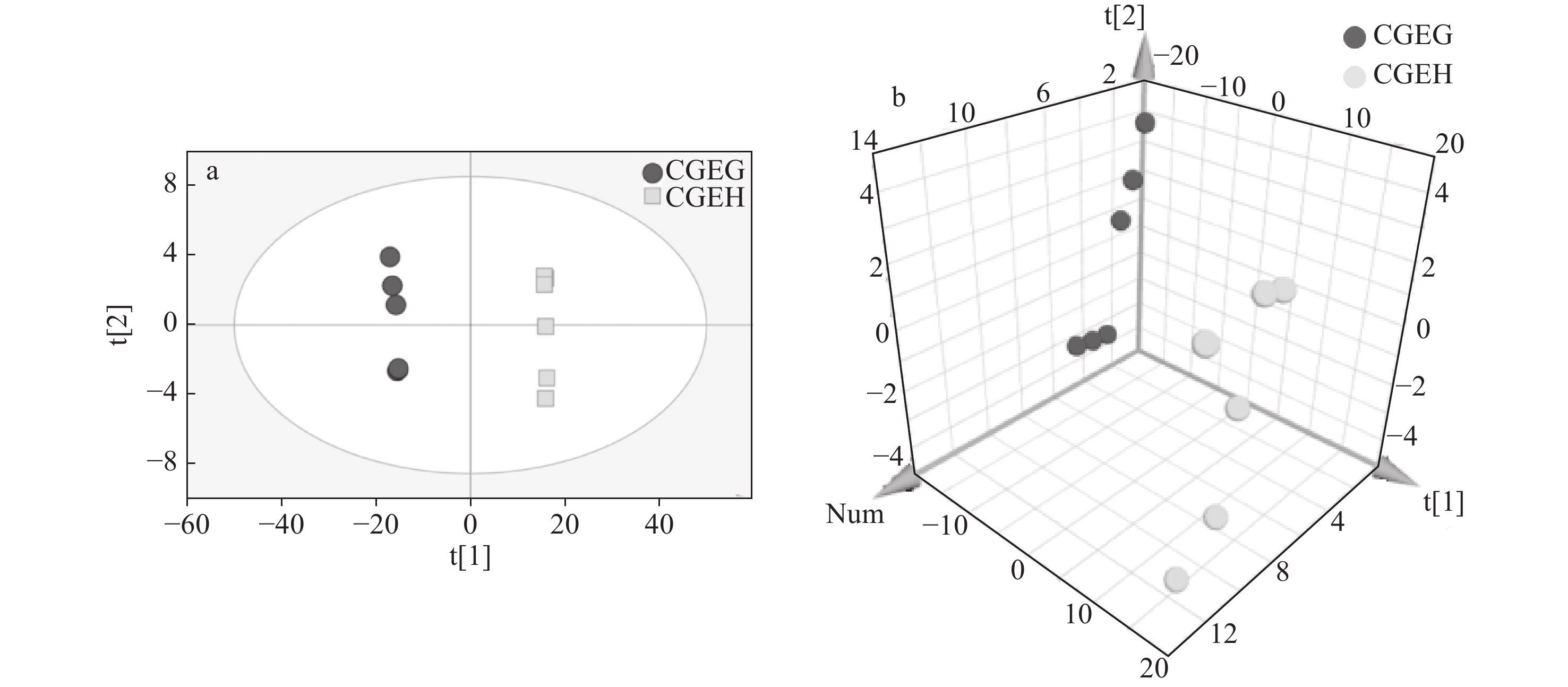
为找出化州橘红与广西橘红的特征成分,对从12个橘红样品中检测到的成分进行PCA,结果示于图4。可以看出,相同产地、不同批次橘红的成分基本无差异,但成分含量存在些许波动。从图4a可以看出,化州橘红和广西橘红所含的挥发性成分存在明显差异。
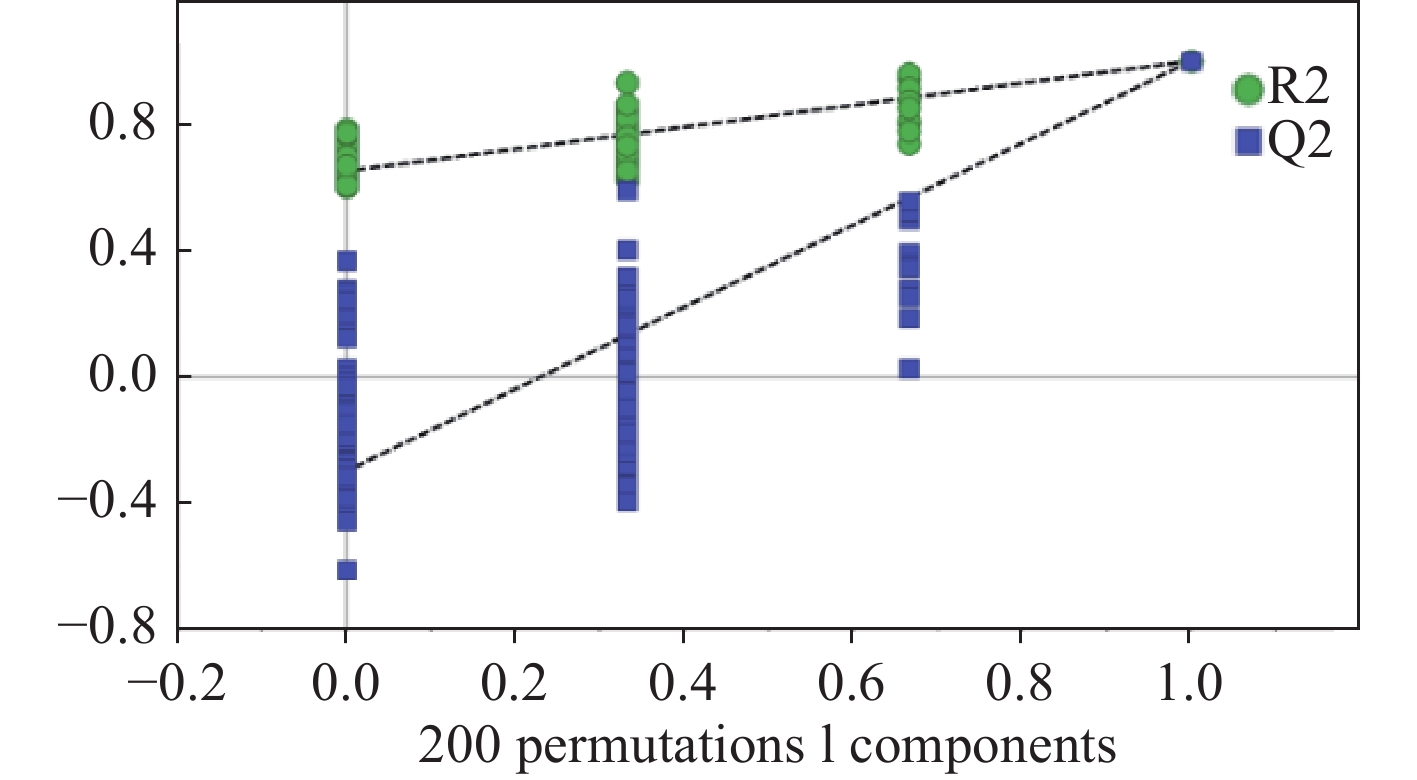
进一步利用OPLS-DA提取模型的变量投影重要度值(VIP),找出|p(corr)|>0.9和|p|>0.06结合VIP>1.1的化合物,共发现了化州橘红中10种特有的挥发性物质,结果列于表3。同时,模型参数R2的模拟值均大于Q2的模拟值,且Q2回归线的截距为−0.45,小于0.718,示于图5,表明模型不存在过拟合现象,证明了数据统计分析的有效性。
-
本研究利用便携GC-MS和顶空固相微萃取与全二维气相色谱-飞行时间质谱相结合分析化州橘红和广西橘红的挥发性成分,发现便携GC-MS只能对2种橘红进行初步鉴别,不能找出差异化合物。对全二维气相色谱-飞行时间质谱的检测数据进行PCA和OPLS-DA;基于 |p(corr)|、p-value与VIP值筛选出化州橘红中含有的10种特征性成分,分别是3,4-二乙基联苯、1-甲基-4-(1-甲基乙烯基)环己烷-1,2-二醇、十二醇、α-亚乙基-苯乙醛、3,8-二甲基-十一烷、十四醛三聚物、2-甲基十三烷、5-甲基-2(5H)-呋喃酮、三缩四乙二醇、沙比诺。本研究可为化州橘红的快速鉴别提供依据,为橘红中有效成分及其香气成分的进一步研究提供基础,同时也为其他中药材的鉴别提供思路。
基于便携GC-MS和HS/SPME-GC×GC-TOF MS分析化州橘红与广西橘红成分差异
Analysis of Composition Differences between Huazhou Citri Grandis Exocarpium and Guangxi Citri Grandis Exocarpium Based on Portable GC-MS and HS/SPME-GC×GC-TOF MS
-
摘要: 为探究不同产地橘红挥发性成分之间的差异,本研究采用便携气相色谱-质谱(GC-MS)和顶空固相微萃取结合全二维气相色谱-飞行时间质谱(GC×GC-TOF MS)技术分析化州橘红和广西橘红的挥发性成分。结果表明,便携GC-MS只能初步区分化州橘红和广西橘红,不能确定化州橘红的特征标志物;利用主成分分析法(PCA)和正交偏最小二乘法(OPLS-DA)对GC×GC-TOF MS实验数据进行处理,根据|p(corr)|>9和|p|>0.06结合VIP>1.1,共筛选出10种化州橘红标志物。该研究为化州橘红药材的质量评价与鉴定提供了依据,也为其他中药质量评价提供了方法参考。
-
关键词:
- 橘红 /
- 便携气相色谱-质谱 /
- 全二维气相色谱-飞行时间质谱(GC×GC-TOF MS) /
- 顶空固相微萃取(HS/SPME) /
- 化学计量学分析
Abstract: The volatile components of Citri Grandis Exocarpium from Huazhou (CGEH) and Guangxi (CGEG) were analyzed by portable gas chromatography-mass spectrometry (GC-MS) and comprehensive two-dimensional gas chromatography-time-of-flight mass spectrometry (GC×GC-TOF MS) combined with headspace solid-phase microextraction (HS/SPME). Due to its limited separation ability, the portable GC-MS can identify only 8 chemicals in CGEH and 4 chemicals in CGEG and is not able to determine any marker compounds which can distinguish CGEH over CGEG. While the merit of GC×GC-TOF MS is strong separation ability, allowing the identification of 304 chemicals in CGEH and CGEG, of which 261 chemicals are reported for the first time. Among them are 52 compounds only detected in CGEH, 81 ones unique in CGEG, and 171 detected in both CGEH and CGEG. The volatile components in CGEH and CGEG are classified into 17 and 19 types, respectively. The contents of alkene aromatics, hydrocarbons and alcohols in both CGEH and CGEG are relatively high. The principal component analysis (PCA) and orthogonal partial least squares (OPLS-DA) were further performed on the MS data obtained by GC×GC-TOF MS. The results indicated that there is basically no difference from different batches of fruits in the same region, while have obvious differences between CGEH and CGEG. Among these different components, 10 compounds including 3,4-diethyl-1,1'-biphenyl, 1-methyl-4-(1-methylethenyl)-1,2-cyclohexanediol, 1-dodecanol, α-ethylidene-benzeneacetaldehyde, 3,8-dimethyl-undecane, tetradecanal, 2-methyl-tridecane, 5-methyl-2(5H)-furanone, tetraethylene glycol, sabinol in CGEH are screened out with the values of Pearson correlation coefficient |p(corr)|>0.9, |p|>0.06 and variable influence on projection (VIP) value>1.1. On the other hand, several marker compounds, such as cedrane, hibaene, 1,3,5-tris(methylene)-cycloheptane, (E)-longipinane, 1,1,6,6-tetramethylspiro[4.4]nonane, 2-(4a,8-dimethyl-1,2,3,4,4a,8a-hexahydro-2-naphthalenyl)-2-propanol, γ-gurjunene, [1S-(1α,4α,7α)]-1,2,3,4,5,6,7,8-octahydro-1,4,9,9-tetramethyl-4,7-methanoazulene, (2R,5S)-2-methyl-5-(prop-1-en-2-yl)-2-vinyltetrahydrofuran, copaene, spathulenol, β-elemene, sativene, N-[4-bromo-n-butyl]-2-piperidinone, eremophilene, 10α-eremophilane, oleyl alcohol, trifluoroacetate, and selinane are picked up in CGEG. These results proved that GC×GC-TOF MS can identify markers of Citri Grandis Exocarpium, while portable GC-MS can not. These markers can help to distinguish CGEH from others and provide references to quality evaluation of Citri Grandis Exocarpium. -

-
表 1 保留指数表
Table 1. List of retention index
序号
No.名称
Name化学式
Chemical formulaCAS号
CAS number一维保留时间
1D retention time/min二维保留时间
2D retention time/s保留指数
Retention index测定值
Actual value文献值[10]
Document value1 癸烷 C10H22 124-18-5 10.61 1.49 1000 1000 2 十一烷 C11H24 1120-21-4 14.11 2.47 1100 1100 3 十二烷 C12H26 112-40-3 18.31 3.05 1200 1200 4 十三烷 C13H28 629-50-5 22.71 3.36 1300 1300 5 十四烷 C14H30 629-59-4 27.01 3.56 1400 1400 6 十五烷 C15H32 629-62-9 31.21 3.67 1500 1500 7 十六烷 C16H34 15716-08-2 35.31 3.72 1600 1600 8 十七烷 C17H36 629-78-7 39.21 3.74 1700 1700 9 十八烷 C18H38 593-45-3 42.91 3.78 1800 1800 10 十九烷 C19H40 629-92-5 46.41 3.85 1900 1900 11 二十烷 C20H42 112-95-8 49.81 3.89 2000 2000 12 二十一烷 C21H44 629-94-7 53.01 3.97 2100 2100 13 二十二烷 C22H46 629-97-0 56.11 4.02 2200 2200 14 二十三烷 C23H48 638-67-5 59.11 4.10 2300 2300 15 二十四烷 C24H50 646-31-1 62.01 4.16 2400 2400 16 二十五烷 C25H52 629-99-2 64.81 4.02 2500 2500 17 二十六烷 C26H54 630-01-3 67.41 4.34 2600 2600 表 2 2种橘红的挥发成分
Table 2. Volatile components of two kinds of Citri Grandis Exocarpium
类别
Category化合物
Compound结构式
Chemical structureCAS号
CAS number保留时间
Retention time/min峰面积
Peak area匹配度
Matching degree化州橘红 月桂烯 
123-35-3 3.163 134523 773 丙基苯 
527-84-4 3.311 13813 806 柠檬烯 
138-86-3 3.328 493213 821 罗勒烯 
13877-91-3 3.368 10057 768 3-蒈烯 
13466-78-9 3.420 56508 848 β-蒎烯 
18172-67-3 3.466 10796 748 2,5-十八碳二炔酸甲酯 
57156-91-9 3.509 27755 633 檀香醇 
115-71-9 4.098 12801 683 广西橘红 月桂烯 
123-35-3 3.159 5703 747 丙基苯 
527-84-4 3.305 5912 784 柠檬烯 
138-86-3 3.324 180133 810 丙烯基甲苯 
7399-49-7 3.507 7247 799 表 3 化州橘红和广西橘红中的特有化合物
Table 3. Specific compounds in CGEH and CGEG
类别
Category序号
No.化合物
CompoundCAS号
CAS numberVIP值
VIP value化州橘红 1 3,4-二乙基联苯
3,4-Diethyl-1,1'-biphenyl61141-66-0 1.56 2 1-甲基-4-(1-甲基乙烯基)环己烷-1,2-二醇
1-Methyl-4-(1-methylethenyl)-1,2-cyclohexanediol1946-00-5 1.50 3 十二醇
1-Dodecanol112-53-8 1.42 4 α-亚乙基-苯乙醛
α-Ethylidene-benzeneacetaldehyde4411-89-6 1.37 5 3,8-二甲基-十一烷
3,8-Dimethyl-undecane17301-30-3 1.33 6 十四醛三聚物
Tetradecanal124-25-4 1.27 7 2-甲基十三烷
2-Methyl-tridecane1560-96-9 1.26 8 5-甲基-2(5H)-呋喃酮
5-Methyl-2(5H)-furanone591-11-7 1.22 9 三缩四乙二醇
Tetraethylene glycol112-60-7 1.22 10 桧醇
Sabinol3310-02-9 1.10 广西橘红 1 雪松烷
Cedrane13567-54-9 1.73 2 亥巴烯
Hibaene2359-73-1 1.67 3 1,3,5-三(亚甲基)环庚烷
1,3,5-tris(Methylene)-cycloheptane68284-24-2 1.64 4 长叶蒎烷
(E)-Longipinane— 1.61 5 四甲基螺[4.4]壬烷
1,1,6,6-Tetramethylspiro[4.4]nonane74054-92-5 1.60 6 六氢-四甲基-萘甲醇
2-(4a,8-Dimethyl-1,2,3,4,4a,8a-hexahydro-2-naphthalenyl)-2-propanol29484-47-7 1.59 7 愈创木二烯
γ-Gurjunene22567-17-5 1.57 8 广藿香烯
[1S-(1α,4α,7α)]-1,2,3,4,5,6,7,8-Octahydro-1,4,9,9-tetramethyl-4,7-methanoazulene514-51-2 1.56 9 2-甲基-5-丙-烯-基-2-乙烯基四氢呋喃
(2R,5S)-2-Methyl-5-(prop-1-en-2-yl)-2-vinyltetrahydrofuran54750-69-5 1.56 10 古巴烯
Copaene18252-44-3 1.56 11 桉油烯醇
Spathulenol6750-60-3 1.56 12 榄香烯
β-Elemene515-13-9 1.55 13 苜蓿烯
Sativene3650-28-0 1.55 14 N-[4-溴正丁基]-2-哌啶酮
N-[4-Bromo-n-butyl]-2-piperidinone195194-80-0 1.54 15 佛术烯
Eremophilene10219-75-7 1.53 16 艾里莫芬烷
10α-Eremophilane3242-05-5 1.52 17 乙酸-唑基醇-三氟酯
Oleyl alcohol-trifluoroacetate— 1.52 18 塞利南
Selinane30824-81-8 1.51 -
[1] 杨建宇, 李杨彦知, 范竹雯, 郑绍明, 柳越冬, 祝庆明, 严雪梅, 陆锦锐, 张朝杰, 张德鸿, 魏素丽, 祝之友. 道地药材化橘红的研究近况[J]. 光明中医, 2020, 35(4): 626 -628 . YANG Jianyu, LI Yangyanzhi, FAN Zhuwen, ZHENG Shaoming, LIU Yuedong, ZHU Qingming, YAN Xuemei, LU Jinrui, ZHANG Chaojie, ZHANG Dehong, WEI Suli, ZHU Zhiyou. Recent research situation of genuine regional drug tangerine[J]. Guangming Journal of Chinese Medicine, 2020, 35(4):626 -628 (in Chinese).[2] 国家药典委员会. 中华人民共和国药典: 一部[M]. 2020年版. 北京: 中国医药科技出版社, 2020. [3] 莫小路, 蔡岳文, 曾庆钱. 中药化橘红的研究进展[J]. 食品与药品, 2007, 9(6): 39 -41 . MO Xiaolu, CAI Yuewen, ZENG Qingqian. Research advance on Citrus Grandis ‘tomentosa’[J]. Food and Drug, 2007, 9(6):39 -41 (in Chinese).[4] 芦海生, 李婷, 姜丹, 孙宇峰, 常晓茜, 胡小松, 刘春生. 基于DNA条形码、UPLC及色度学方法鉴定与评价化橘红[J]. 中国中药杂志, 2019, 44(20): 4 419-4 425. LU Haisheng, LI Ting, JIANG Dan, SUN Yufeng, CHANG Xiaoxi, HU Xiaosong, LIU Chunsheng. Identification and evaluation of Citrus grandis based on DNA barcode, UPLC and chromaticity method[J]. China Journal of Chinese Materia Medica, 2019, 44(20): 4 419-4 425(in Chinese). [5] 高泽林, 张晓营, 麦宝愉, 林霞婷, 方家祺, 钟嘉锐, 詹若挺, 肖凤霞. 不同基原和规格化橘红的质量差异分析[J]. 中国药房, 2022, 33(7): 825 -829 . doi: 10.6039/j.issn.1001-0408.2022.07.10 GAO Zelin, ZHANG Xiaoying, MAI Baoyu, LIN Xiating, FANG Jiaqi, ZHONG Jiarui, ZHAN Ruoting, XIAO Fengxia. Analysis of quality difference of different specifications and different origins of Citri grandis exocarpium[J]. China Pharmacy, 2022, 33(7):825 -829 (in Chinese). doi: 10.6039/j.issn.1001-0408.2022.07.10[6] 王晓峰, 陈德斌, 刘美, 覃睿, 江泽权, 黄小琼, 甘凤琼, 李良波, 黄荣韶. 利用GC-MS法测定不同产地化橘红的挥发油成分[J]. 大众科技, 2019, 21(10): 32 -34, 76 . WANG Xiaofeng, CHEN Debin, LIU Mei, QIN Rui, JIANG Zequan, HUANG Xiaoqiong, GAN Fengqiong, LI Liangbo, HUANG Rongshao. Using GC-MS method to determine the volatile oil composition of Citrus Grandis tomentosa in different origin[J]. Popular Science & Technology, 2019, 21(10):32 -34, 76 (in Chinese).[7] 周伟明, 刘浩, 郑海. 基于HS-SPME-GC-MS快速分析毛橘红和光橘红挥发性成分[J]. 黑龙江医药, 2022, 35(4): 745 -747 . ZHOU Weiming, LIU Hao, ZHENG Hai. Rapid analysis of volatile substances in Citrus Grandis ‘tomentosa’ and Citrus grandis (L.) osbeck based on HS-SPME-GC-MS[J]. Heilongjiang Medicine Journal, 2022, 35(4):745 -747 (in Chinese).[8] 周伟明, 刘浩, 王玲, 梁颖, 郑海. 基于近红外与主成分分析化橘红的快速无损鉴别[J]. 海峡药学, 2020, 32(11): 55 -58 . doi: 10.3969/j.issn.1006-3765.2020.11.017 ZHOU Weiming, LIU Hao, WANG Ling, LIANG Ying, ZHENG Hai. Rapid and non-destructive identify Citri grandis exocarpium by NIRs and PCA[J]. Strait Pharmaceutical Journal, 2020, 32(11):55 -58 (in Chinese). doi: 10.3969/j.issn.1006-3765.2020.11.017[9] 李沃颖, 卢思捷. 使用全二维气相色谱-飞行时间质谱仪分析茶叶挥发性香味成份探究[J]. 广东化工, 2022, 49(23): 223 -226 . doi: 10.3969/j.issn.1007-1865.2022.23.072 LI Woying, LU Sijie. Analysis of volatile aroma components of tea by full two-dimensional gas chromatography-time of flight mass spectrometer[J]. Guangdong Chemical Industry, 2022, 49(23):223 -226 (in Chinese). doi: 10.3969/j.issn.1007-1865.2022.23.072[10] LU X, ZHU X, GAO R, TANG H, PEI C, WANG H, XIAO J. Chemometrics-assisted analysis of chemical impurity profiles of tabun nerve agent using comprehensive two-dimensional gas chromatography-time-of-flight mass spectrometry[J]. Journal of Chromatography A, 2022, 1 685: 463 643. [11] 国家医药管理局中草药情报中心站. 植物有效成分手册[M]. 北京: 人民卫生出版社, 1986: 668-669. [12] VIEIRA A J, BESERRA F P, SOUZA M C, TOTTI B M, ROZZA A L. Limonene: aroma of innovation in health and disease[J]. Chemico-Biological Interactions, 2018, 283: 97 -106 . doi: 10.1016/j.cbi.2018.02.007[13] 樊钰虎, 周刚, 张璐, 陈小燕, 李翠萍. 连钱草挥发油化学成分的气相色谱-质谱分析[J]. 中国实验方剂学杂志, 2010, 16(13): 41 -44 . doi: 10.3969/j.issn.1005-9903.2010.13.012 FAN Yuhu, ZHOU Gang, ZHANG Lu, CHEN Xiaoyan, LI Cuiping. Analysis on chemical components of volatile oils from glechoma longituba by gas chromatography-mass spectrometry[J]. Chinese Journal of Experimental Traditional Medical Formulae, 2010, 16(13):41 -44 (in Chinese). doi: 10.3969/j.issn.1005-9903.2010.13.012[14] 唐小江, 黄华容, 方铁铮, 杨翠平, 张援, 吴邦华, 许实波. 毛大丁草根止咳化痰活性成分的研究[J]. 中国中药杂志, 2003, 28(5): 426 -429 . doi: 10.3321/j.issn:1001-5302.2003.05.012 TANG Xiaojiang, HUANG Huarong, FANG Tiezheng, YANG Cuiping, ZHANG Yuan, WU Banghua, XU Shibo. The antitussive and de-sputum essential substance from the root of Gerbera piloselloides and its analytical compositions[J]. China Journal of Chinese Materia Medica, 2003, 28(5):426 -429 (in Chinese). doi: 10.3321/j.issn:1001-5302.2003.05.012[15] TANG Q, XU F, WEI X, GU J, QIAO P, ZHU X, YIN S, OUYANG D, DONG J, YAO J, WANG Y, CHEN J. Investigation of β-caryophyllene as terpene penetration enhancer: role of stratum corneum retention[J]. Eur J Pharm Sci, 2023, 183: 106 401. [16] 卫洁, 孙斌, 王立志, 张广军, 李新, 郭鸽, 陈祥, 卢鹏, 张凯. 2,3,5-三甲基吡嗪的合成研究进展[J]. 山东化工, 2014, 43(9): 32 -34 . WEI Jie, SUN Bin, WANG Lizhi, ZHANG Guangjun, LI Xin, GUO Ge, CHEN Xiang, LU Peng, ZHANG Kai. Progress in synthesis of 2,3,5-trimethylpyrazine[J]. Shandong Chemical Industry, 2014, 43(9):32 -34 (in Chinese).[17] JALALVAND A R. Chemometrics in investigation of small molecule-biomacromolecule interactions: a review[J]. International Journal of Biological Macromolecules, 2021, 181: 478 -493 . doi: 10.1016/j.ijbiomac.2021.03.184[18] HUANG Y, WU Z, SU R, RUAN G, DU F, LI G. Current application of chemometrics in traditional Chinese herbal medicine research[J]. Journal of Chromatography B, 2016, 1 026: 27-35. [19] COZZOLINO D, POWER A, CHAPMAN J. Interpreting and reporting principal component analysis in food science analysis and beyond[J]. Food Analytical Methods, 2019, 12(11): 2 469-2 473. [20] MEHMOOD T, AHMED B. The diversity in the applications of partial least squares: an overview[J]. Journal of Chemometrics, 2016, 30(1): 4 -17 . doi: 10.1002/cem.2762 -


 首页
首页 登录
登录 注册
注册


 下载:
下载: