-
癌症是世界范围内备受关注的公共卫生问题,其发病率与死亡率长期居高不下[1]。在我国,2022年新增癌症确诊病例482.47万人,死亡病例257.42万人[2]。癌症的早期发现对患者的生存和生活质量具有重要意义,不仅能够降低癌症的死亡率,在某些情况下,尽早干预甚至仅需简单治疗即可获得理想的预后效果。然而,目前癌症的早期筛查手段仍未能达到预期效果[3]。
髓母细胞瘤(medulloblastoma,MB)是一种可发生在大脑任何部位的胚胎源性肿瘤,是儿童最常见的恶性脑肿瘤,其患儿数量约占儿童脑肿瘤患者的30%,具有极高的致死率和极差的预后。世界卫生组织(WHO)在中枢神经系统肿瘤分级中将其列为WHO IV级,表明该肿瘤在组织学上具有高度恶性特征[4-6]。但针对髓母细胞瘤的准确诊断仍是目前面临的重要临床难题[7]。因此,筛选髓母细胞瘤的特征生物标志物并进行精确定量,对于疾病的早期诊断及治疗指导具有重要的临床意义。
生物标志物是可用于测量、评估或指示生物体状态的物质或特征,主要包括蛋白质、核酸、多肽及一系列有机小分子化学物质[8]。生物标志物在评估机体功能或定量诊断中具有重要作用,能够提供关于一种或多种特定疾病发生的潜在机制信息。这些标志物通常可指示疾病的发展和演变趋势,被用作药物靶标[9-10]。目前,已有多种生物标志物应用于临床实践,临床上通常采取对生物标志物的定性或定量分析,实现癌症的诊断、预后和治疗[11-12]。然而,已知的生物标志物在检测灵敏度和诊断特异性等方面存在一系列问题,因此,亟需建立新的检测方法,以实现对肿瘤代谢标志物更快速、更灵敏的筛查与检测。
髓母细胞瘤生物标志物的鉴定通常采用非靶向代谢组学分析方法[13]。然而,该方法在代谢物识别的准确性和可信度方面存在局限,且重复性较差、线性范围较窄,可能导致假阳性结果[13]。为解决这一问题,首都医科大学附属世纪坛医院研究团队对髓母细胞瘤患者血浆样本中的全谱氨基酸进行了靶向代谢组学分析[14]。该研究利用相应的标准品对氨基酸进行精确的定性定量分析,最终筛选出髓母细胞瘤患者血浆中的4种氨基酸生物标志物,包括亮氨酸(Leu)、苯丙氨酸(Phe)、酪氨酸(Tyr)和胱氨酸(Cys)[14]。目前,在新生儿疾病筛查[15]、临床25-羟基维生素D定量分析[16-17]、类固醇类激素检测[18]、血药浓度监测[19-20]等方面,四极杆-线形离子阱质谱展现出显著优势。
本研究采用课题组自主研制的QLIT-6610MD四极杆-线形离子阱液相色谱-质谱联用仪[15],建立血浆中氨基酸标志物的检测方法。其中,QLIT-6610MD使用一种基于Q-LIT质谱的同步碎裂和累积技术(简称“同步技术”),可以克服杂质离子对目标离子稳定存储和精确操控的干扰,降低基质效应并有效抑制空间电荷效应[16]。为提高检测的灵敏度与准确度,血浆样品经蛋白沉淀后进行衍生化处理。其中,胱氨酸采用外标法定量分析,亮氨酸、苯丙氨酸、酪氨酸采用同位素稀释质谱法定量分析。
-
QLIT-6610MD液相色谱-串联质谱系统:安徽砺沐医疗器械有限公司产品;AB QTRAP 6500+液相色谱-串联质谱系统:美国AB Sciex公司产品;VORTEX-GENE2涡旋混合器:美国Scientific Industries公司产品;G20型高速医用离心机:北京白洋医疗器械有限公司产品;Sigma 3K15高速离心机:德国Sigma公司产品;Sartorius BT 125D电子天平:德国赛多利斯集团产品;恒温金属浴振荡混匀器:杭州米欧仪器有限公司产品;DGG-9146A电热恒温鼓风干燥箱:上海精密试验设备有限公司产品;KQ-600DE型数控声波清洗器:昆山市超声仪器有限公司产品;冰箱:韩国LG公司产品;Five Easy Plus pH计:梅特勒-托利多仪器(上海)有限公司产品;微量可调移液器:德国Eppendorf公司产品;Phenomenex Kinetex C18色谱柱(150 mm×2.1 mm,2.6 μm):美国Phenomenex公司产品。
亮氨酸(纯度99.8%)、苯丙氨酸(纯度99.7%)、酪氨酸(纯度99.4%)标准物质:购自中国计量科学研究院;胱氨酸:德国Sigma公司产品;亮氨酸-D7、苯丙氨酸-D10、酪氨酸-D10标准品:加拿大TRC公司产品;6-氨基喹啉基-N-羟基琥珀酰亚胺基甲酸酯(AQC):上海麦克林生化科技股份有限公司产品;甲醇、乙腈、甲酸、超纯水:均为质谱级,美国Thermo Fisher公司产品。
-
血浆样本:来自首都医科大学附属北京世纪坛医院。本研究方案经首都医科大学附属北京世纪坛医院科学研究伦理委员会批准(伦理号sjtky11-1x-2021(21))。所有参与者均提供书面知情同意书,其中包含37例髓母细胞瘤患者血浆样本、23例正常人血浆样本。
为确保样品的稳定性,混合人血浆样本的容量不少于500 μL,干冰运输,且于−80 ℃保存。使用前,样品在室温平衡1 h。
-
由于所测氨基酸均为内源性组分,无法获取空白血浆溶液,基于氨基酸的溶解度,本实验采用50%乙腈水溶液作为溶剂配制标准品溶液。
-
称定各1 mg 胱氨酸、亮氨酸、苯丙氨酸、酪氨酸标准品,加入50%乙腈水溶液,涡旋混匀,配制成浓度为1 000 μmol/L标准储备液,分装,于−20 ℃避光保存。临用前,用50%乙腈水溶液稀释成浓度分别为1、2、4、10、20、40、100、200、400 μmol/L的工作液。
-
称定1 mg氨基酸同位素混标,用50%乙腈水溶液溶解,得到1 000 μmol/L储备液,分装,于−30 ℃避光保存。
-
制备3、30、300 μmol/L QC工作液。
-
称定1 mg AQC试剂,用1 mL 乙腈溶解,得到1 000 mg/L衍生化试剂储备液。使用前于55 ℃孵育不少于15 min。
-
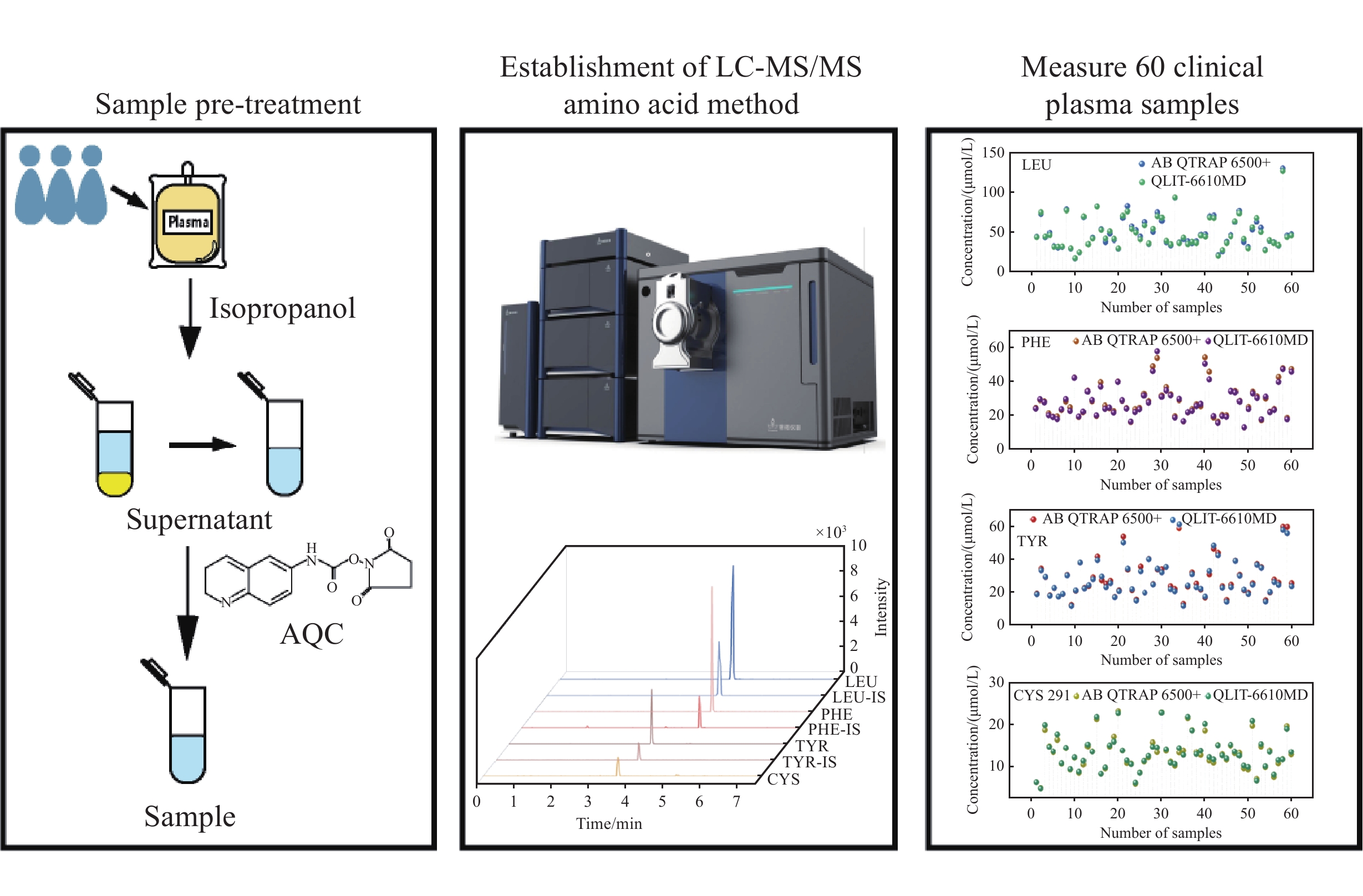
向10 μL血浆样本中加入10 μL水和5 μL内标,适当混匀,加入40 μL异丙醇,振荡10~20 min,沉淀蛋白。于4 ℃以12 000 r/min离心15 min,取10 μL上清液于1.5 mL离心管中,加入70 μL硼酸盐缓冲液,调至pH 8~10,再加入20 μL衍生试剂溶液,迅速振荡10 s。待反应1 min(确保衍生完全)后,用过量的衍生剂水解,衍生反应结束;将离心管放在55 ℃加热装置中加热10 min。样品衍生完毕,加入900 μL水稀释,上机检测。
-
色谱条件:Phenomenex Kinetex C18色谱柱(150 mm×2.1 mm,2.6 μm),柱温45 ℃;流动相为0.1%甲酸水溶液(A)和0.1%甲酸乙腈溶液(B),流速0.6 mL/min;进样器温度4 ℃;进样量3 μL;梯度洗脱程序:0~0.5 min(96%A),0.5~2.5 min(96%~90%A),2.5~5.0 min(90%~72%A),5.0~5.1 min(72%~5%A),5.1~6.1 min(5%A),6.1~6.2 min(5%~96%A),6.2~7.2 min(96%A)。
质谱条件:电喷雾离子源正离子模式,子离子扫描(QTPIS)与多级子离子扫描(QTPISn);电喷雾电压4 500 V,离子源温度350 ℃,大气压接口温度300 ℃,鞘气压强4.14×105 Pa,辅助气压强2.07×105 Pa,反吹气压强5.52×105 Pa,其他质谱参数列于表1。
-
色谱条件同1.5.1节。质谱条件:电喷雾离子源正离子模式,多反应监测(MRM)模式;电喷雾电压5 500 V,离子源温度450 ℃,雾化气压强3.79×105 Pa,辅助加热气压强3.45×105 Pa,气帘气压强2.41×105 Pa,碰撞解离气Medium,其他质谱参数列于表2。
-
在本研究中,由于样本量有限、血浆基质复杂且待测物为内源性物质,无法获取空白血浆,从而难以配制基质匹配标准曲线进行定量分析。为克服这一问题并最大程度降低基质效应对检测结果的影响,本研究采用AQC试剂对血浆样品中的待测氨基酸进行衍生化处理。该方法[21]的氨基酸衍生效率可达90%以上,适用于小体积生物样本的定量分析。
AQC试剂可与伯胺和仲胺按1:1比例发生反应。AQC氨基酸衍生化示意图示于图1,过量的AQC试剂与水反应可生成6-氨基喹啉(AMQ),AMQ可与过量的AQC试剂缓慢反应形成双脲。这些衍生物不会干扰肽或蛋白质水解产物中氨基酸的分离、鉴定和定量分析。由于衍生物在数天内能够保持稳定,因此可以进行批处理或者重复分析。
-
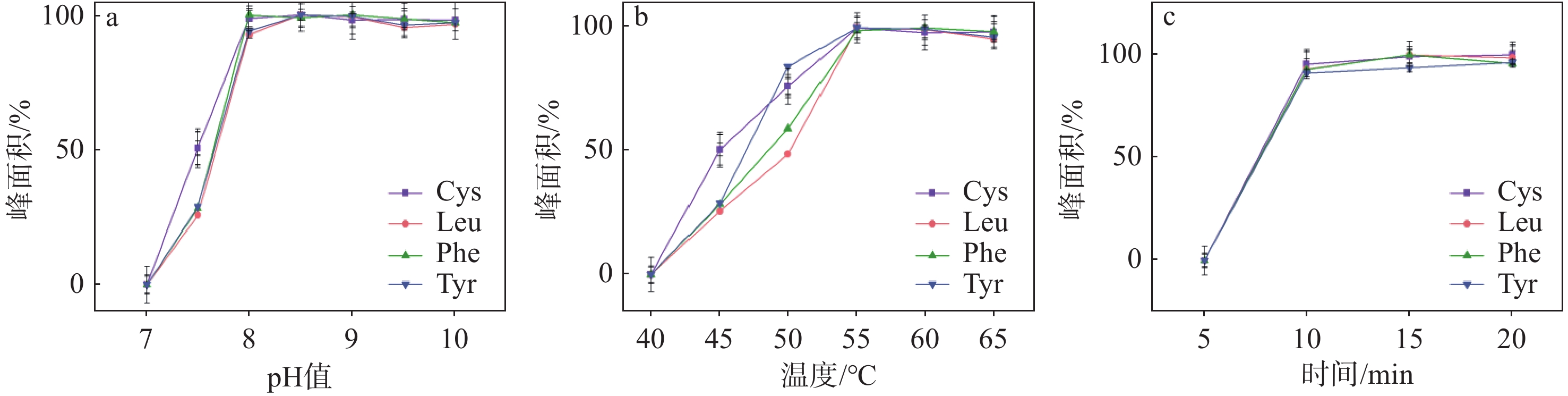
取10 μL 100 μmol/L 4种氨基酸标准品溶液于1.5 mL离心管中,边振荡边加入70 μL硼酸盐缓冲液和20 μL 1 000 mg/L衍生试剂溶液,使用0.5 mol/L NaOH与0.5 mol/L HCl将pH值分别调至7、7.5、8、8.5、9、9.5、10,迅速振荡10 s。待反应1 min后,使用过量的衍生剂水解,将离心管于60 ℃加热装置中加热15 min。样品衍生完毕后加入900 μL水稀释,上机检测,结果示于图2a。可见,在pH 8~10范围内,4种氨基酸均可获得较好的衍生化效果,加入70 μL硼酸盐缓冲液即可满足衍生化反应pH值的要求。
-
取10 μL 100 μmol/L 4种氨基酸标准品溶液于1.5 mL离心管中,边振荡边加入70 μL硼酸盐缓冲液和20 μL 1 000 mg/L衍生试剂溶液,迅速振荡10 s。待反应1 min后,使用过量的衍生剂水解,将离心管分别置于40、45、50、55、60、65 ℃加热装置中加热15 min。样品衍生完毕后加入900 μL水稀释,上机检测,结果示于图2b。可见,在55 ℃时,4种目标氨基酸的峰面积达到最高值;在55~65 ℃范围内,峰面积的变化不明显。因此,最佳的衍生化温度应不低于55 ℃。
-
取10 μL 100 μmol/L 4种氨基酸标准品溶液于1.5 mL离心管中,边振荡边加入70 μL硼酸盐缓冲液和20 μL 1 000 mg/L衍生试剂溶液,迅速振荡10 s。待反应1 min后,使用过量的衍生剂水解,将离心管置于55 ℃加热装置中加热5、10、15、20 min。样品衍生完毕后加入900 μL水稀释,上机检测,结果示于图2c。可见,在衍生化时间10~20 min之间,4种氨基酸的峰面积变化不明显,且远大于衍生化时间5 min的峰面积。因此,氨基酸衍生化时间至少需要10 min。
-
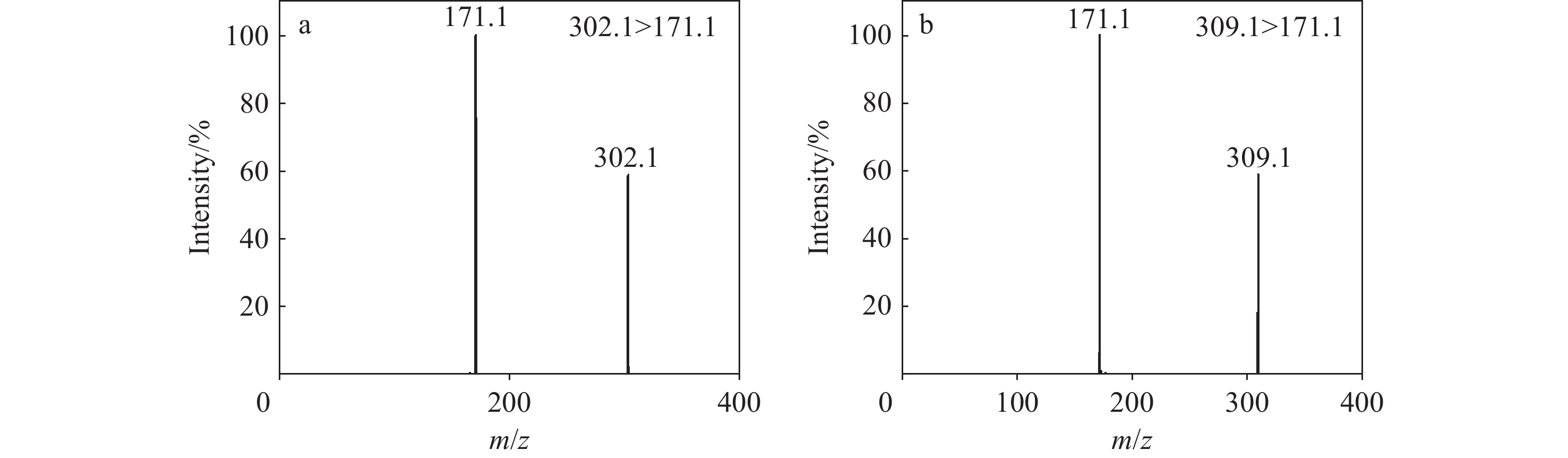
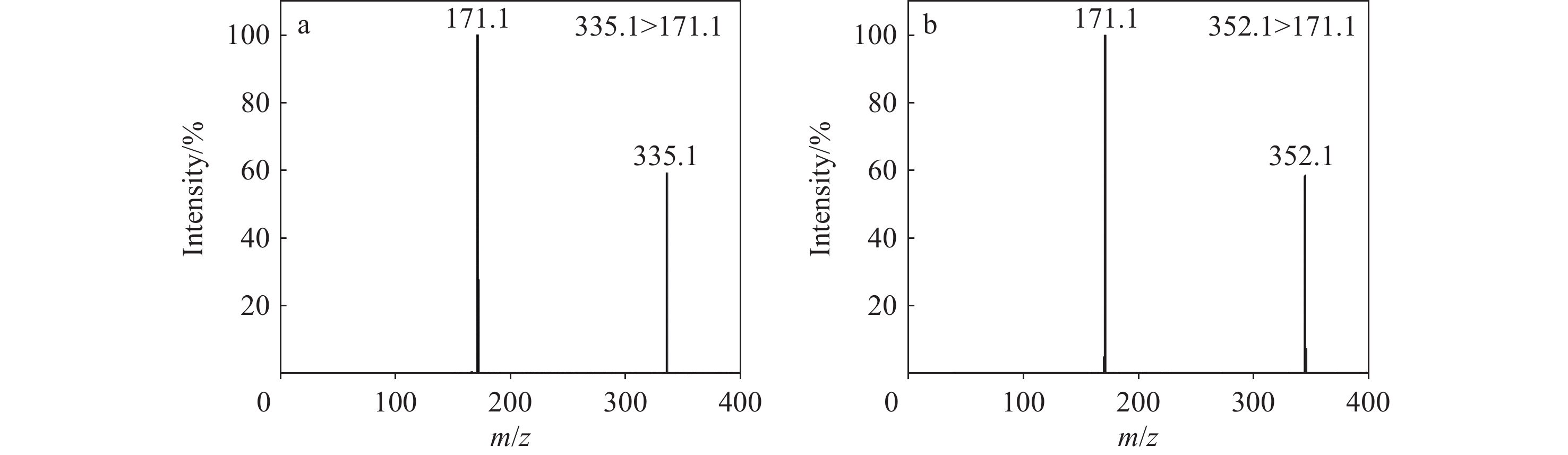
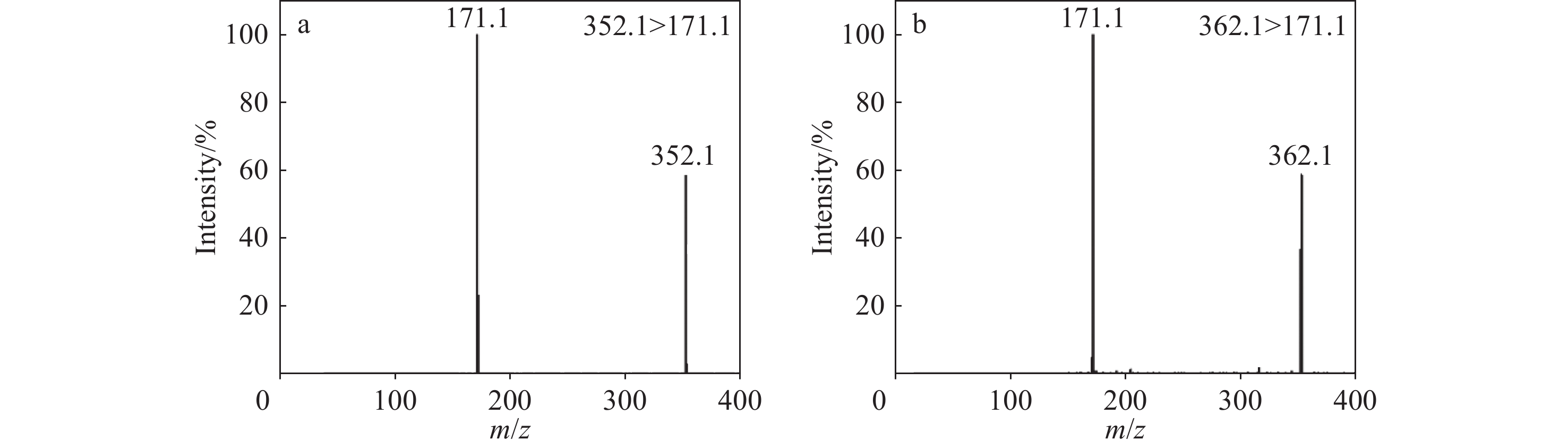
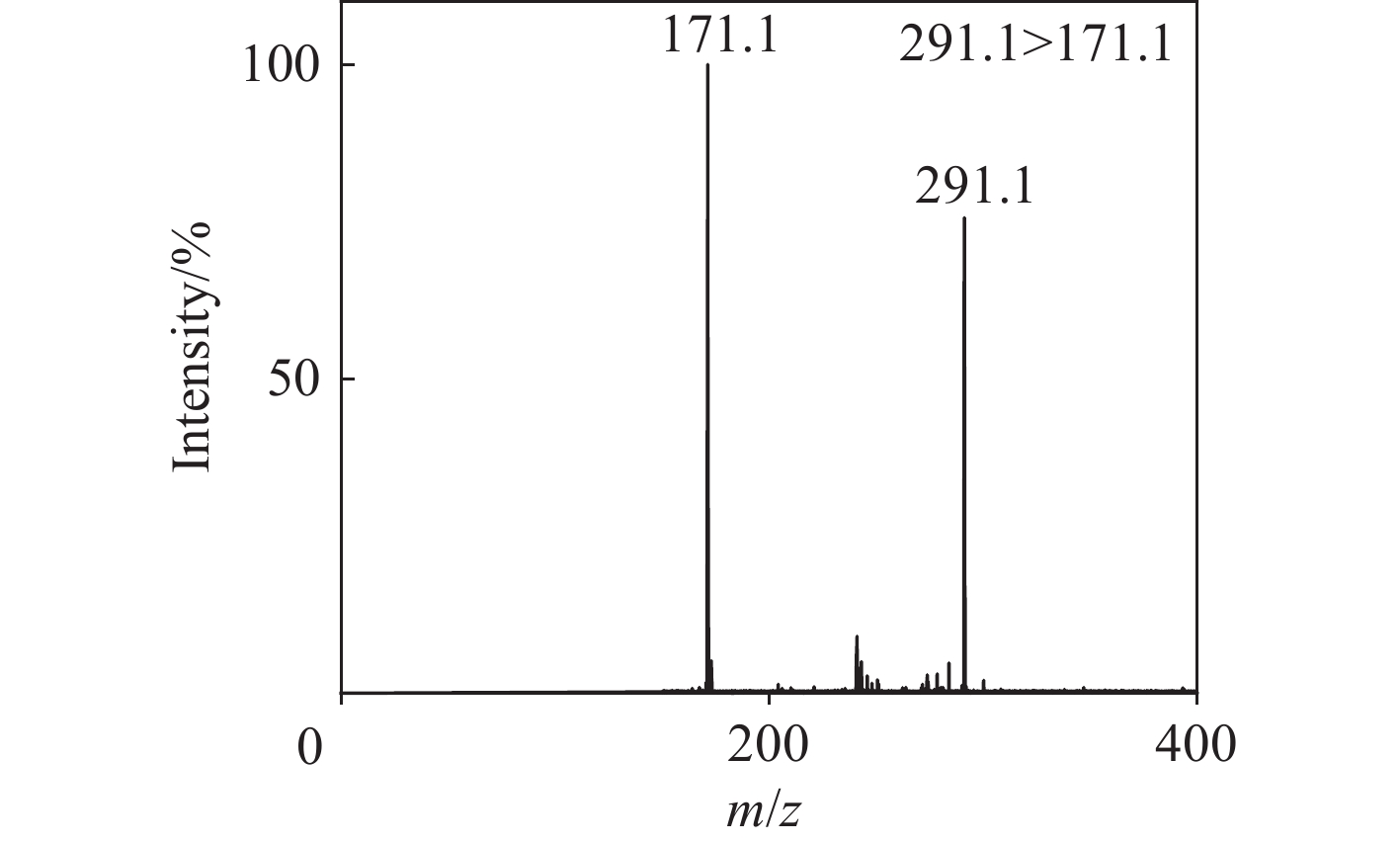
使用外置注射泵在5 μL/min流速下流动注射10 μmol/L经衍生化处理的4种氨基酸及其内标的混合标准溶液,正离子模式扫描分析。衍生化反应后,单胺类氨基酸会与单个AQC反应生成单一衍生物,在正离子模式下形成[M+AQC+H]+离子;而部分多胺类(如胱氨酸、赖氨酸)由于具有多个反应位点,可产生多个AQC加合物。经分析,4种氨基酸在m/z 50~40扫描范围内的基峰均为[M+AQC+H]+,具体为m/z 291.1(胱氨酸);m/z 302.1(亮氨酸)、m/z 309.1(亮氨酸-d7);m/z 335.1(苯丙氨酸)、m/z 345.1(苯丙氨酸-d10);m/z 352.1(酪氨酸)、m/z 362.1(酪氨酸-d10)。
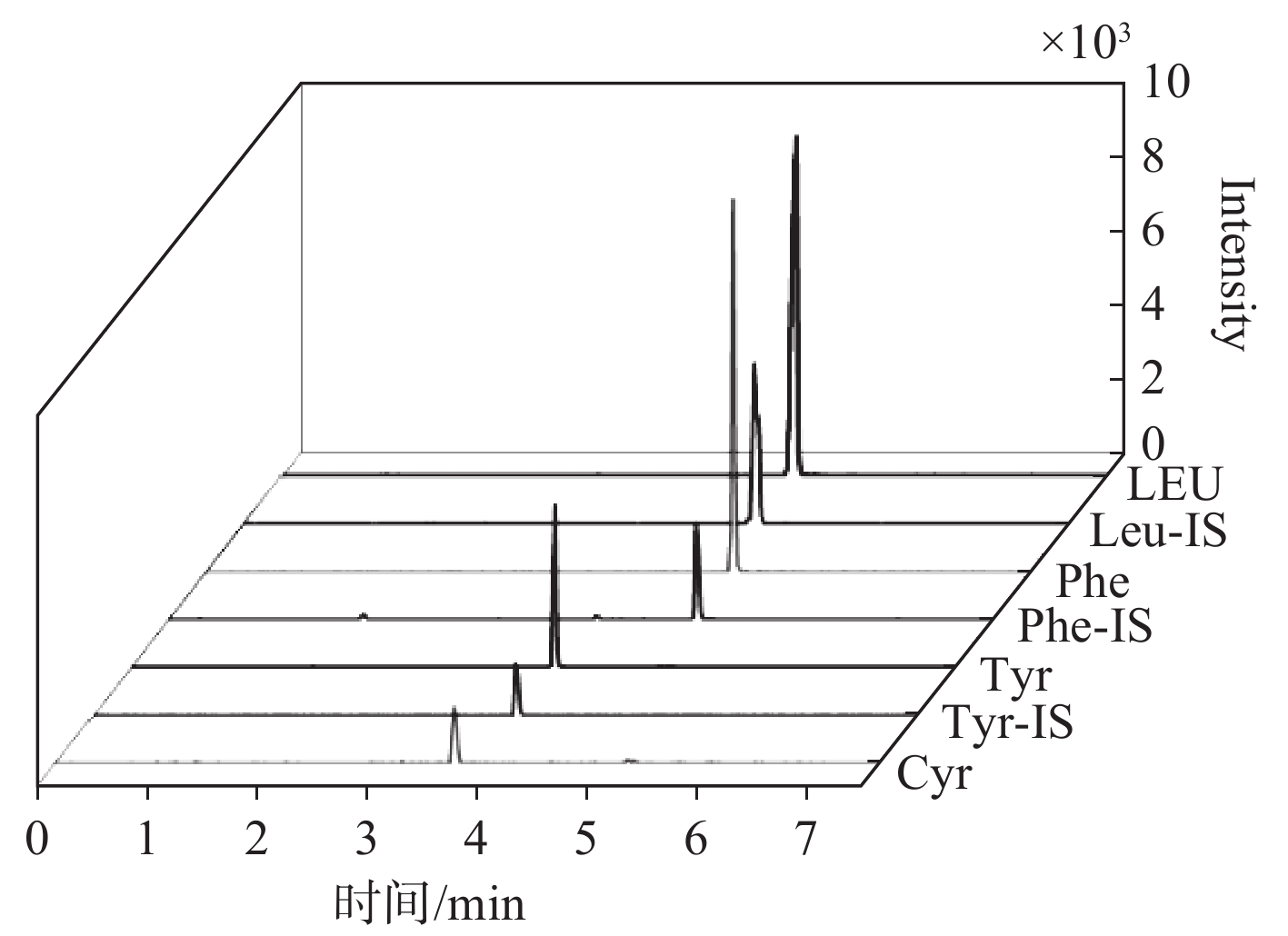
分别对4种氨基酸及其内标的母离子施加一定的碎裂能量,得到的二级质谱图示于图3~6。可知,4种氨基酸及其同位素内标的子离子均为m/z 171.1,这是由于氨基酸衍生化后,AQC试剂会产生1个共同的片段离子m/z 171.1,该离子由AMQ分子的损失产生。在先前的研究[21]中,通常选择由母离子和这一共同片段组成的离子对进行检测。因此,确定4种氨基酸及其内标的定量离子对分别为:m/z 291.1>171.1(胱氨酸);m/z 302.1>171.1(亮氨酸)、m/z 309.1>171.1(亮氨酸-d7);m/z 335.1>171.1(苯丙氨酸)、m/z 345.1>171.1(苯丙氨酸-d10);m/z 352.1>171.1(酪氨酸)、m/z 362.1>171.1(酪氨酸-d10)。优化后的提取离子色谱图示于图7。
-
取10 μL水,加入10 μL氨基酸混标工作溶液,按1.4节方法进行前处理及衍生化。以胱氨酸待测成分峰面积为纵坐标(y),待测成分浓度为横坐标(x);以亮氨酸、苯丙氨酸、酪氨酸待测成分与内标成分的峰面积比值为纵坐标(y),待测成分浓度为横坐标(x),得到标准曲线,具体结果及线性范围列于表3。4种氨基酸的线性关系良好,胱氨酸的线性相关系数(R2)为
0.9979 ,亮氨酸、苯丙氨酸、酪氨酸的R2≥0.9935 。 -
以10倍信噪比作为定量限(LOQ),且满足重复测定5次峰面积相对标准偏差(RSD)≤15%,4种氨基酸的LOQ为1 μmol/L,RSD≤7.81%。
-
将10 μL超纯水放入离心管中,随后加入10 μL QC工作液和5 μL内标溶液,配制低、中、高3个浓度的QC质控样品,然后按照1.4节方法进行样品处理和衍生化。在同一天内,对每个浓度的样品制备5份,连续进样,以获得日内精密度和准确度;连续3天,每天制备5份样品,综合3批结果得出日间精密度和准确度,结果列于表4。可知,精密度变异系数(CV)值均小于15%,相对偏差在±15%范围内。
-
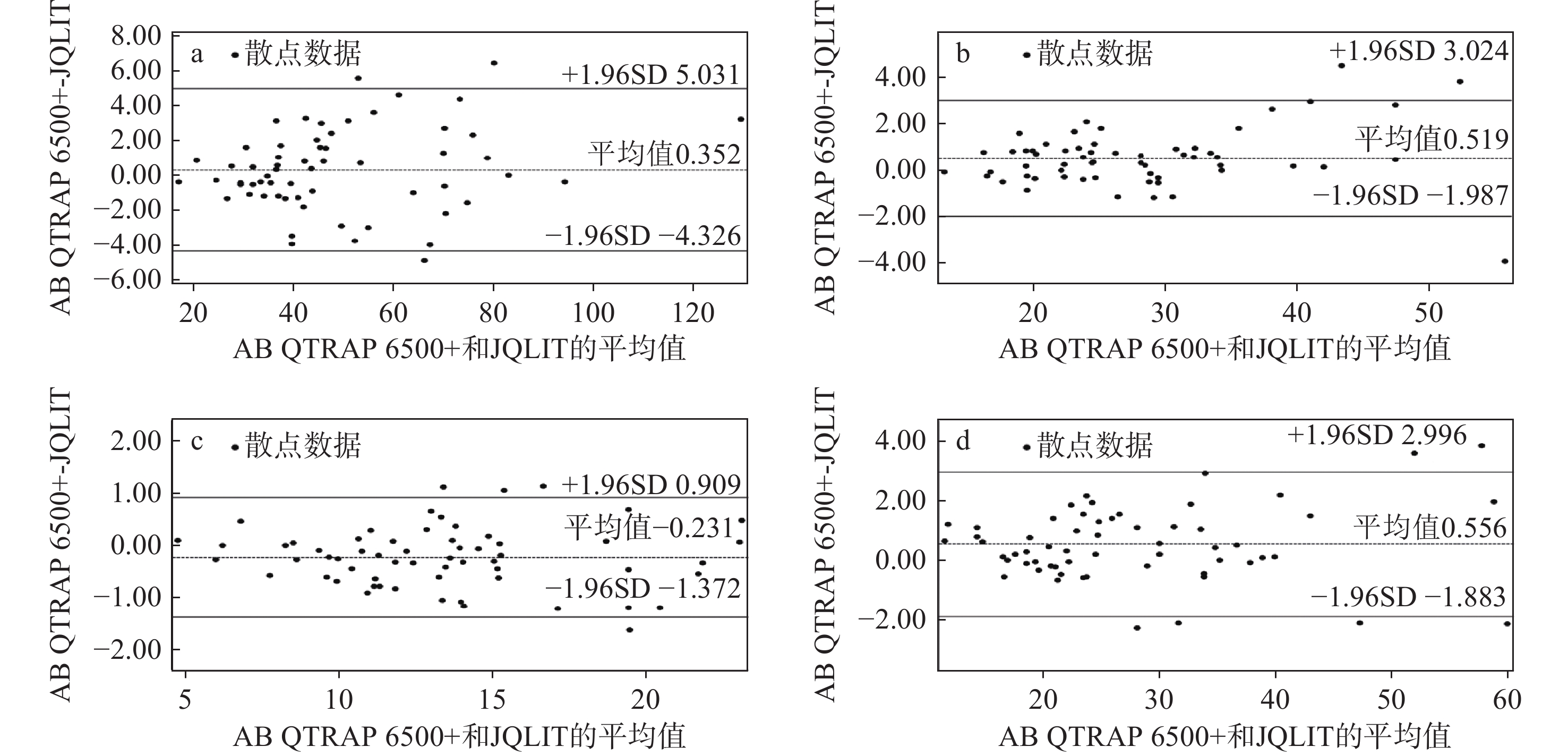
本实验分别采用QLIT-6610MD和AB QTRAP 6500+液质联用仪测定60例人血浆样本中的胱氨酸、亮氨酸、苯丙氨酸、酪氨酸,其含量分别为4.70~22.97、17.16~127.06、13.21~57.89、11.14~60.97 μmol/L。通过Pearson相关系数分析发现,QLIT-6610MD和AB QTRAP 6500+之间的相关系数(R)达0.996以上,表明存在显著正相关(P<0.01)。进一步采用Bland-Altman法分析数据一致性,数据界外点的百分比均不超过10%,结果示于图8、9。表明两者之间的数据一致性较好,可靠性较高。
-
本研究基于自主研制的液相色谱-四极杆-线形离子阱串联质谱仪建立了血浆氨基酸检测方法,准确定量分析了髓母细胞瘤血浆中胱氨酸、亮氨酸、苯丙氨酸、酪氨酸等4种氨基酸生物标志物。使用AQC试剂氨基酸进行衍生化,以目标氨基酸待测物峰面积为指标,对衍生化体系的pH值、温度、时间进行优化。结果表明,当pH值为8~10、衍生化温度不低于55 ℃、衍生化时间不低于10 min时,氨基酸衍生化效率最高。实验测定了60例实际血浆样本中4种氨基酸生物标志物,胱氨酸、亮氨酸、苯丙氨酸、酪氨酸的含量分别为4.70~22.97、17.16~127.06、13.21~57.89、11.14~60.97 μmol/L。采用Pearson系数分析QLIT-6610MD和有证进口商业仪器检测的60例实际血清样本,2台仪器所测数据显著相关。通过Bland-Altman法分析表明,该数据具有良好的一致性,能够满足临床监测需求。本方法适用于检测氨基酸小分子疾病标志物,可为临床髓母细胞瘤以及相关疾病生物标志物的监测提供可行高效的国产仪器选择。
基于四极杆-线形离子阱串联质谱研究髓母细胞瘤氨基酸生物标志物定量分析方法
Quantitative Analysis of Amino Acid Biomarkers for Medulloblastoma Based on Quadrupole-Linear Ion Trap Isotope Dilution Mass Spectrometry
-
摘要: 本研究基于自主研制的QLIT-6610MD四极杆-线形离子阱液相色谱-质谱联用仪,建立了血浆中髓母细胞瘤氨基酸生物标志物(亮氨酸、苯丙氨酸、酪氨酸、胱氨酸)的准确定量分析方法。采用异丙醇沉淀血浆样品蛋白,6-氨基喹啉基-N-羟基琥珀酰亚胺基甲酸酯(AQC)对上清液进行氨基酸衍生化后,使用QLIT-6610MD四极杆-线形离子阱串联质谱仪进行定量检测。采用同位素内标法对亮氨酸、苯丙氨酸、酪氨酸进行定量分析,在1~400 μmol/L浓度范围内的线性关系良好,相关系数(R2)分别为
0.9964 、0.9935 、0.9995 ,定量限为1 μmol/L,质控品精密度均小于15%,准确度均在±14%范围内;采用外标法对胱氨酸进行定量分析,定量限为1 μmol/L,在1~400 μmol/L浓度范围内的R2≥0.9979 ,质控品精密度在1.2%~11.6%之间,准确度在−7.4%~10.8%范围内。使用QLIT-6610MD和AB QTRAP 6500+两台液相色谱-质谱联用仪测定60例临床血浆样本,其中,亮氨酸、苯丙氨酸、酪氨酸、胱氨酸含量分别为17.16~127.06、13.21~57.89、11.14~60.97、4.70~22.97 μmol/L。采用Pearson系数分析数据相关性,QLIT-6610MD和AB QTRAP 6500+之间的相关系数(R)≥0.996,两者呈显著正相关(P<0.01);采用Bland-Altman分析数据一致性,数据界外点数百分比均≤10%,表明数据一致性良好。该方法能够满足临床实际监测的需求。-
关键词:
- 液相色谱-串联质谱(LC-MS/MS) /
- 四极杆-线形离子阱质谱 /
- 生物标志物 /
- 髓母细胞瘤 /
- 氨基酸
Abstract: A method of liquid chromatography-tandem mass spectrometry (LC-MS/MS) was developed based on the self-developed QLIT-6610MD quadrupole-linear ion trap liquid chromatography-mass spectrometry for the accurate quantification of amino acid biomarkers including leucine, phenylalanine, tyrosine, and cystine in plasma for medulloblastoma research. Plasma samples were processed by proteins precipitation with isopropanol, and the supernatant was quantified using a QLIT-6610MD quadrupole-linear ion trap tandem mass spectrometer after amino acid derivatization with 6-aminoquinolinyl-N-hydroxysuccinimidylformate (AQC). Leucine, phenylalanine and tyrosine were quantified by an isotope internal standard method, and the linearity is good in the range of 1-400 μmol/L with the determination coefficients (R2) of0.9964 ,0.9935 ,0.9995 , respectively, and the limit of quantification (LOQ) is 1 μmol/L. The precision of the quality control samples is less than 15%, and the accuracies are within the range of ±14%. Cystine was quantified by an external standard method, the LOQ is 1 μmol/L, and R2 of the target is not less than0.9979 in the range of 1-400 μmol/L, and the precision of the quality control samples ranges from 1.2% to 11.6%, the accuracy is within the range of −7.4% to 10.8%. Two liquid chromatography-mass spectrometry instruments, QLIT-6610MD and AB QTRAP 6500+, were used to analyze 60 clinical plasma samples, in which the concentrations of leucine, phenylalanine, tyrosine, cystineis are in the range of 17.16-127.06, 13.21-57.89, 11.14-60.97, 4.70-22.97 μmol/L, respectively. Data correlation was analyzed using the Pearson coefficient, and the correlation coefficient (R) between QLIT-6610MD and AB QTRAP 6500+ is ≥0.996, indicating a significant positive correlation (P<0.01). Data consistency was analyzed using Bland-Altman, and the percentage of data out-of-bounds points is ≤10%, indicating that the data consistency is good and meets the actual clinical monitoring needs. -

-
表 1 QLIT-6610MD质谱参数
Table 1. Mass spectrometry parameters of QLIT-6610MD
氨基酸
Amino acid母离子
Parent ion (m/z)子离子
Product ion (m/z)碎裂能量
Fragmentation energy/%碎裂q点
q Point离子化时间
Ionization time/sLeu 302.1 171.1 25 0.28 0.01 Leu-d7 309.1 171.1 25 0.28 0.01 Phe 335.1 171.1 25 0.3 0.01 Phe-d10 345.1 171.1 25 0.3 0.01 Tyr 352.1 171.1 25 0.3 0.01 Tyr-d10 362.1 171.1 25 0.3 0.01 Cys 291.1 171.1 25 0.35 0.3 表 2 AB QTRAP 6500+ 质谱参数
Table 2. Mass spectrometry parameters of AB QTRAP 6500+
氨基酸
Amino acid母离子
Parent ion (m/z)子离子
Product ion (m/z)去簇电压
Decluster potential/V碰撞能量
Collision energy/V驻留时间
Dwell time/sLeu 302.1 171.1 50 34 0.01 Leu-d7 309.1 171.1 50 31 0.01 Phe 335.1 171.1 50 38 0.01 Phe-d10 345.1 171.1 50 30 0.01 Tyr 352.1 171.1 50 34 0.01 Tyr-d10 362.1 171.1 50 38 0.01 Cys 291.1 171.1 50 23 0.01 表 3 4种氨基酸的线性关系与定量限
Table 3. Linear relationship and limit of quantification of 4 amino acids
氨基酸
Amino acid标准曲线
Calibration curve相关系数
Correlation coefficient (R2)线性范围
Linearity range/(μmol/L)定量限
LOQ/(μmol/L)Cys y=32539.6x+672.523 0.9979 1~400 1 Leu y=0.117283x+0.0134711 0.9964 1~400 1 Phe y=0.346144x+0.0254845 0.9935 1~400 1 Tyr y=0.936181x+0.0753799 0.9995 1~400 1 表 4 4种氨基酸的准确度与精密度
Table 4. Accuracy and precision of 4 amino acids
氨基酸
Amino acid理论浓度
Theoretical concentration/
(μmol/L)日内精密度
Intra-day precision
(n=5)日间精密度
Inter-day precision
(n=5)实际浓度
Actual concentration/
(μmol/L)相对偏差
Relative
deviation/%变异
系数
CV/%实际浓度
Actual concentration/
(μmol/L)相对偏差
Relative
deviation/%变异
系数
CV/%Cys 3 3.22 7.2 7.2 2.81 10.8 11.6 30 29.04 −3.2 5.1 29.44 −0.6 9.7 300 278.41 −7.2 5.0 277.83 −7.4 12.3 Leu 3 2.77 −7.7 11.6 2.91 −2.9 7.6 30 27.84 −7.2 3.2 29.04 −3.2 6.2 300 269.39 −10.2 7.1 280.84 −6.4 6.9 Phe 3 2.72 −9.5 16 2.95 −1.8 14.4 30 27.96 −6.8 2.5 28.77 −4.1 3.6 300 266.41 −11.2 7.1 273.95 −8.7 7.0 Tyr 3 2.82 −6.0 8.0 2.69 −10.3 8.8 30 28.08 −6.4 4.4 28.77 −4.1 4.7 300 267.93 −10.7 5.7 274.80 −8.4 7.1 -
[1] 赵平, 邹小农, 隋晨光, 李纪宾, 裴力峰. 中国癌症态势及防控战略研究[C]. 2015第八届世界癌症大会会刊, 北京, 2015: 393. [2] HAN B, ZHENG R, ZENG H, WANG S, SUN K, CHEN R, LI L, WEI W, HE J. Cancer incidence and mortality in China, 2022[J]. Journal of the National Cancer Center, 2024, 4(1): 47 -53 . doi: 10.1016/j.jncc.2024.01.006[3] SCHIFFMAN J D, FISHER P G, GIBBS P. Early detection of cancer: past, present, and future[C]. American Society of Clinical Oncology Educational Book American Society of Clinical Oncology Annual Meeting, 2015: 57-65. [4] PDQ Pediatric Treatment Editorial Board. Childhood medulloblastoma and other central nervous system embryonal tumors treatment (PDQ®): health professional version[M]. Bethesda: National Cancer Institute, 2002. [5] NORTHCOTT P A, ROBINSON G W, KRATZ C P, MABBOTT D J, POMEROY S L, CLIFFORD S C, RUTKOWSKI S, ELLISON D W, MALKIN D, TAYLOR M D, GAJJAR A, PFISTER S M. Medulloblastoma[J]. Nature Reviews Disease Primers, 2019, 5: 11 . doi: 10.1038/s41572-019-0063-6[6] SIDAWAY P. Medulloblastoma: prognostic subtypes revealed[J]. Nat Rev Clin Oncol, 2021, 18(3): 131 . doi: 10.1038/s41571-021-00478-0[7] SUK Y, GWYNNE W D, BURNS I, VENUGOPAL C, SINGH S K. Childhood medulloblastoma: an overview[J]. Methods Mol Biol, 2022, 2 423: 1-12. [8] LUDWIG J A, WEINSTEIN J N. Biomarkers in cancer staging, prognosis and treatment selection[J]. Nat Rev Cancer, 2005, 5(11): 845 -856 . doi: 10.1038/nrc1739[9] FITZGERALD G A. Measure for measure: biomarker standards and transparency[J]. Sci Transl Med, 2016, 8(343): 343fs10 .[10] KHALILPOUR A, KILIC T, KHALILPOUR S, ÁLVAREZ M M, YAZDI I K. Proteomic-based biomarker discovery for development of next generation diagnostics[J]. Applied Microbiology and Biotechnology, 2017, 101(2): 475 -491 . doi: 10.1007/s00253-016-8029-z[11] LI J, LI J, WANG H, QI L W, ZHU Y, LAI M. Tyrosine and glutamine-leucine are metabolic markers of early-stage colorectal cancers[J]. Gastroenterology, 2019, 157(1): 257 -259 . doi: 10.1053/j.gastro.2019.03.020[12] MARRERO J A, FENG Z. Alpha-fetoprotein in early hepatocellular carcinoma[J]. Gastroenterology, 2010, 138(1): 400 -401 . doi: 10.1053/j.gastro.2009.08.076[13] 姜文, 田璐肖, 智静驿, 甄晓兰, 李挥, 哈婧. 液质联用技术在肿瘤诊断与监测中的应用进展[J]. 中国医院药学杂志, 2023, 43(15): 1 752-1 757. JIANG Wen, TIAN Luxiao, ZHI Jingyi, ZHEN Xiaolan, LI Hui, HA Jing. Advances in the application of LC-MS/MS in tumor diagnosis and monitoring[J]. Chinese Journal of Hospital Pharmacy, 2023, 43(15): 1 752-1 757 (in Chinese). [14] SHI Z, YANG C, XU X, WU W, JIANG D, YAN D. Plasma metabolite profiles identify pediatric medulloblastoma and other brain cancer[J]. Analytical and Bioanalytical Chemistry, 2023, 415(3): 471 -480 . doi: 10.1007/s00216-022-04427-3[15] FANG X, XIE J, CHU S, JIANG Y, AN Y, LI C, GONG X, ZHAI R, HUANG Z, QIU C, DAI X. Quadrupole-linear ion trap tandem mass spectrometry system for clinical biomarker analysis[J]. Engineering, 2022, 16: 56 -64 . doi: 10.1016/j.eng.2020.10.021[16] 李畅, 谢洁, 刘梅英, 黄泽建, 戴新华, 江游, 方向, 田地. 基于四极杆-双压线形离子阱质谱的同步碎裂和累积技术研究[J]. 分析化学, 2023, 51(2): 269 -275 . LI Chang, XIE Jie, LIU Meiying, HUANG Zejian, DAI Xinhua, JIANG You, FANG Xiang, TIAN Di. Study on synchronous fragmentation and accumulation technology based on quadrupole-dual-pressure linear ion trap mass spectrometry[J]. Chinese Journal of Analytical Chemistry, 2023, 51(2):269 -275 (in Chinese).[17] 谢洁, 易可可, 高文静, 刘浩, 李家练, 黄泽建, 刘梅英, 余青霓, 王涵文, 江游, 戴新华, 方向. 基于四极杆-线形离子阱串联质谱技术测量血清25OHD[J]. 质谱学报, 2023, 44(1): 13 -24 . doi: 10.7538/zpxb.2022.0103 XIE Jie, YI Keke, GAO Wenjing, LIU Hao, LI Jialian, HUANG Zejian, LIU Meiying, YU Qingni, WANG Hanwen, JIANG You, DAI Xinhua, FANG Xiang. Determination of 25OHD in serum based on quadrupole-linear ion trap tandem mass spectrometric technique[J]. Journal of Chinese Mass Spectrometry Society, 2023, 44(1):13 -24 (in Chinese). doi: 10.7538/zpxb.2022.0103[18] 万薇, 谢洁, 屈子裕, 江游, 张谛, 黄泽建, 王一楠, 戴新华, 方向, 叶子弘. 基于LC-MS/MS测定人体类固醇激素的研究进展[J]. 质谱学报, 2024, 45(2): 201 -215 . doi: 10.7538/zpxb.2023.0073 WAN Wei, XIE Jie, QU Ziyu, JIANG You, ZHANG Di, HUANG Zejian, WANG Yinan, DAI Xinhua, FANG Xiang, YE Zihong. Research progress in the determination of human steroid hormones based on LC-MS/MS[J]. Journal of Chinese Mass Spectrometry Society, 2024, 45(2):201 -215 (in Chinese). doi: 10.7538/zpxb.2023.0073[19] 谢洁, 李姿颖, 屈子裕, 易可可, 刘浩, 李家练, 张谛, 黄泽建, 王涵文, 时正媛, 鄢丹, 俞晓平, 江游, 戴新华, 方向. 四极杆-线形离子阱串联质谱法测量血清中万古霉素[J]. 质谱学报, 2023, 44(5): 602 -613 . doi: 10.7538/zpxb.2023.0017 XIE Jie, LI Ziying, QU Ziyu, YI Keke, LIU Hao, LI Jialian, ZHANG Di, HUANG Zejian, WANG Hanwen, SHI Zhengyuan, YAN Dan, YU Xiaoping, JIANG You, DAI Xinhua, FANG Xiang. Determination of vancomycin in serum by quadrupole-linear ion trap tandem mass spectrometry[J]. Journal of Chinese Mass Spectrometry Society, 2023, 44(5):602 -613 (in Chinese). doi: 10.7538/zpxb.2023.0017[20] 刘粮泽, 谢洁, 屈子裕, 易可可, 张谛, 黄泽建, 鄢丹, 戴新华, 方向, 时正媛, 江游, 俞晓平. 自主研制四极杆-线形离子阱质谱仪测定血清中甲氨蝶呤[J]. 质谱学报, 2024, 45(3): 364 -374 . doi: 10.7538/zpxb.2023.0082 LIU Liangze, XIE Jie, QU Ziyu, YI Keke, ZHANG Di, HUANG Zejian, YAN Dan, DAI Xinhua, FANG Xiang, SHI Zhengyuan, JIANG You, YU Xiaoping. Determination of methotrexate in serum by house-made quadrupole-linear ion trap mass spectrometer[J]. Journal of Chinese Mass Spectrometry Society, 2024, 45(3):364 -374 (in Chinese). doi: 10.7538/zpxb.2023.0082[21] GRAY N, ZIA R, KING A, PATEL V C, WENDON J, MCPHAIL M J, COEN M, PLUMB R S, WILSON I D, NICHOLSON J K. High-speed quantitative UPLC-MS analysis of multiple amines in human plasma and serum via precolumn derivatization with 6-aminoquinolyl-N-hydroxysuccinimidyl carbamate: application to acetaminophen-induced liver failure[J]. Anal Chem, 2017, 89(4): 2 478-2 487. -


 首页
首页 登录
登录 注册
注册
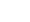


 下载:
下载: