-
中国是生产抗生素的第一大国,每天都会有大使用。然而抗生素在人体或动物体内使用后,其未被生物体利用的部分将以尿液或粪便的形式由母体结构排出进入生态环境中,从而影响生态平衡。Dong等[1]在对城市地下水中抗生素进行取样时发现磺胺类,林可酰胺类、大环内酯类和四环素类是下水道系统中最常见的四类抗生素且平均浓度分别达到1246 ng/L、 2418 ng/L、 1734 ng/L、 1140 ng/L。因抗生素其难降解性,使得其在排放到污水管网前必须先进行预处理以防止危害地下水安全,因此迫切需要研发一种新的技术对水体中的抗生素进行治理显得尤为重要。
化石燃料虽然对人类社会的快速发展做出了突出的贡献,但其燃烧过程中会产生温室气体二氧化碳,由于排放的二氧化碳超过了自然界的碳循环,且2022年大气中测得的二氧化碳浓度已经达到421 ppm。这就迫切需要有效利用二氧化碳,这样不仅可以减少温室气体排放,而且可以更好地利用碳资源。因此近年来,二氧化碳的捕获和利用引起了科学研究人员的广泛关注[2-4]。
低温等离子体因其可在放电区产生各种强氧化活性物质,已被广泛应用于环境污染控制、材料制备和生物医学领域[5-7]。近年来,低温等离子体作为一种成熟的水处理技术,由于其高效和非选择性,被广泛应用于降解抗生素和其他难降解有机污染物。其中等离子体在气液界面活性物质的高效产生和输运并与液相中的抗生素快速作用,从而提高降解效率是需考虑的重点问题。因此,空气、氧气、氮气、氩气、氦气及其混合气被用作工作气氛,生成所需的活性物质(如reactive oxygen species, ROS;reactive nitrogen species, RNS),以满足不同的应用要求并提高处理效率[8]。研究人员亦采用等离子体协同催化剂,充分利用等离子体-催化体系引发的气液相物理、化学效应,产生更多活性物质,以提高污染物的去除效率[9]。或者采用水膜式等离子体反应装置,以提高等离子体与水溶液的反应界面,促进活性物质的产生及活性物质的气液气液传质过程,从而提高体系的降解效率[10]。
本研究以CO2/Ar作为载气,产生气液相等离子体,尝试从等离子体CO2转化、活性氧原子、·OH等活性物质产生等不同影响因素,继而研究其对液相盐酸四环素(Tetracycline hydrochloride, TC)降解机理。分析了气液相等离子体物理特性:电流电压、放电形态、发射光谱、二氧化碳转化以及二氧化碳转化可能的影响因素,如CO2/Ar比例、总气体流量;随后具体研究了化学特性,首先分析了TC降解的影响因素,如CO2/Ar比例、TC初始浓度、总气体流量以及初始pH对TC降解的影响。最后分析了CO2/Ar等离子放电体系产生的不同活性物质,以及其降解TC可能的降解途径。以期利用气态污染物CO2处理液相污染物TC,为CO2利用以及水污染治理提供了一个新的思路。
-
图1描述了气液相等离子体的装置的示意图。等离子装置由中空的金属针电极组成,针周围环绕着内径为3.5 mm的石英玻璃管,管的一端紧紧固定。针不仅用作阳极电极,由高压直流电源驱动,还连接到气体入口。阳极电极末端距石英玻璃管出口20 mm,接地电极安装在反应器的侧壁上。反应气体通过中空电极进入,经高压激发,等离子体在高压电极和气液通道间产生。采用高速相机捕捉CO2/Ar气液相等离子体放电羽流形态,曝光时间为20 ns,拍摄频率为50 fps。
-
在实验中,二氧化碳(高纯度二氧化碳,99.995%)和Ar载气的流量分别由流量控制器控制,总气体流量为300 mL/min,产生的气体通过排气管利用气袋进行收集,随后通过气相色谱仪(FULI 9790 II)对产生的CO进行检测,从而得出CO2转化率。20 mL的TC溶液被添加到玻璃容器中,溶液与固定在侧壁的电极接触作为接地极,在放电区产生活性基团以及高能电子进入溶液中与TC发生反应。本次研究在气液相等离子体不同时间点分别取样,通过紫外分光光度计(SHIMADZU, UV2700)在356 nm下分析TC浓度。二氧化碳转化率(
$ \varphi $ ),TC降解率($ \eta $ )通过以下式(1)和式(2)计算得到:式中:D0,Dt为初始CO2体积分数和反应后(未加入TC)CO体积分数,单位 ppm;
$ \varphi $ 为二氧化碳转化率。式中:C0,Ct为TC初始浓度和经过t时间处理后TC的浓度,单位 mg/L;
$ \eta $ 为TC降解率。 -
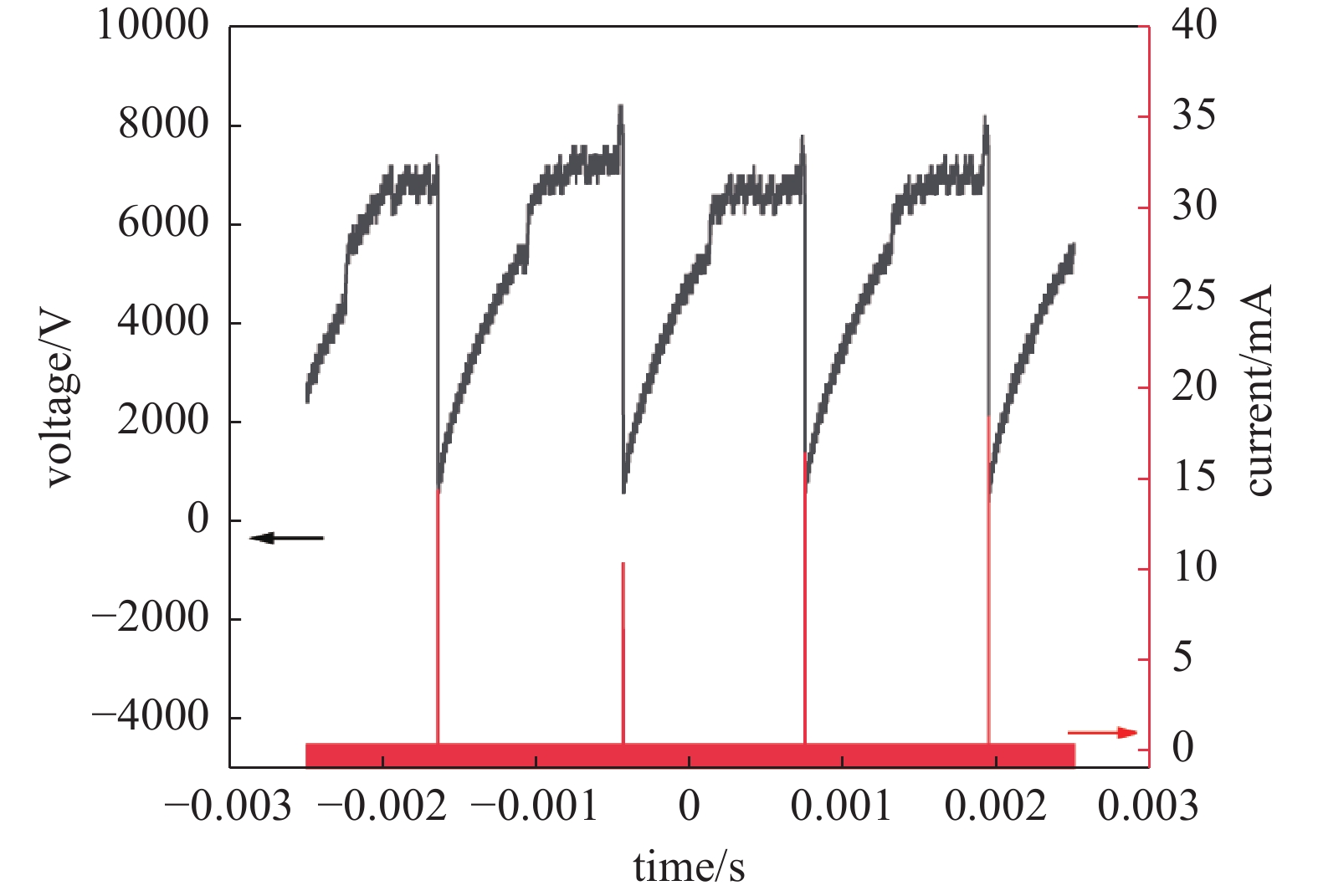
如图1所示,在周期性电压、电流尖脉冲作用下,CO2/Ar气液相等离子体在玻璃管内、气液界面呈现出丝状放电形态。等离子体与液体直接接触,同时在气流作用下,有利于产生的活性物质高效输运至液相中。
图2为CO2/Ar气液相等离子体电流、电压波形图。气液相等离子体放电呈周期性变化,当放电电压逐渐增加到击穿电压时,激发气液相的等离子体放电,产生周期性电流尖脉冲,峰值电压为8.43 kV,峰值电流为18.45 mA。放电功率大约为0.7 W。
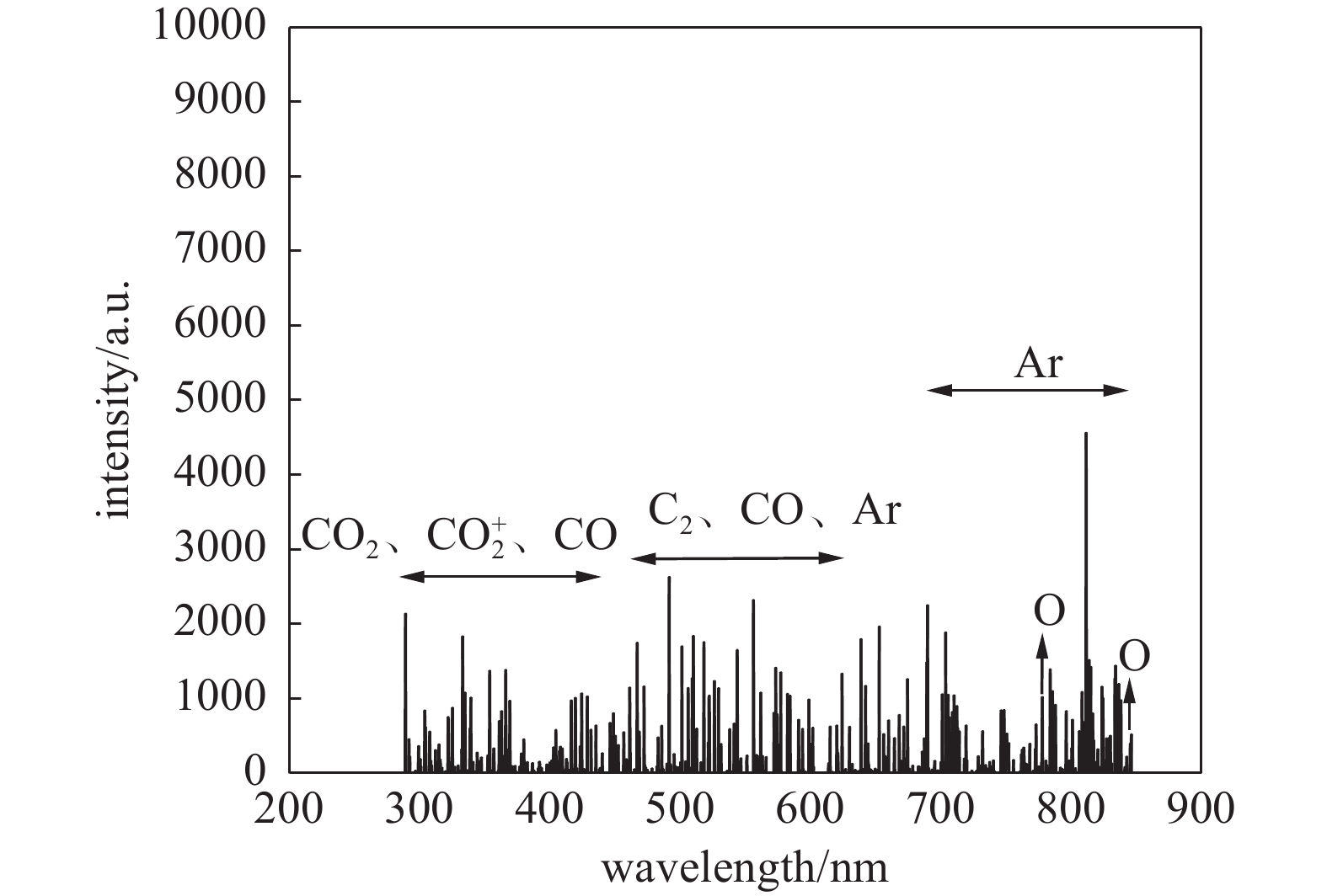
发射光谱仪常用于测定等离子体放电区产生的激发态活性物质。本研究中,氩气的加入可以降低击穿电压,并使气液相放电过程更加稳定。在等离子体放电区内,Ar原子因具有较高的激发电离能级而被激发或电离,从而增加CO2电子碰撞解离的概率[11]。图3显示了CO2/Ar气液相等离子发射光谱图,其谱线主要是由CO、C2 (430-610 nm)、CO2+ (351.1、367.4、385.2、404.7、410.9、434.2 nm)、Ar (696.5、706.7、738.4、750.4、751.5、763.5、772.4、826.5 nm) 及活性氧原子 (777.6 nm、844.6 nm)组成[12]。光谱中激发态原子、分子及电子和离子,在气液相接触面引发一系列的物理和化学过程,有利于各类活性物质的生成。
-
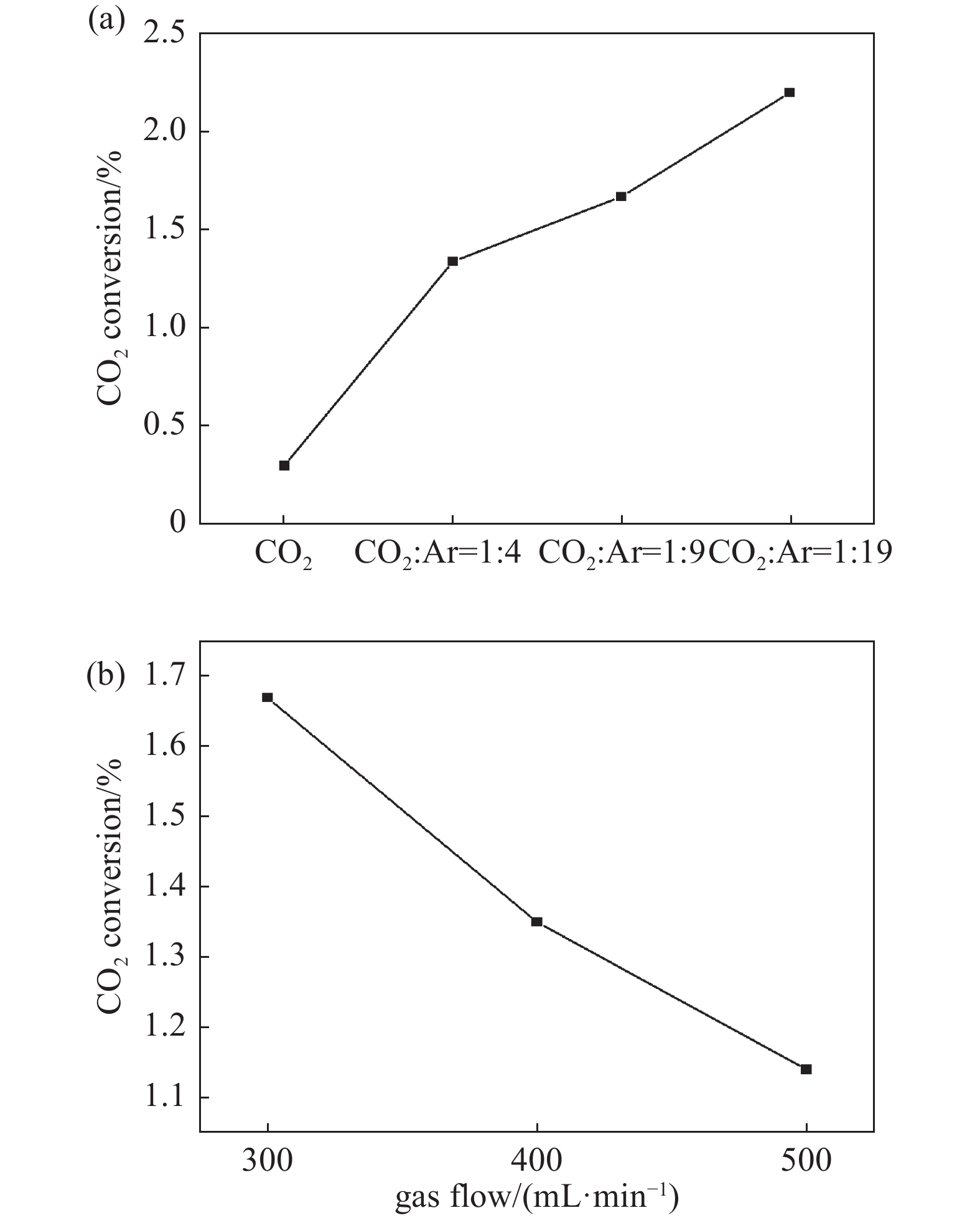
为研究CO2/Ar气液相等离子体CO2转化率,本实验利用气相色谱仪对产生的CO气体进行检测,并以(公式2)对CO2转化率进行计算,本文探究了不同CO2与Ar的比例对CO2转化的影响。如图4(a)所示,随着Ar参比的提高,CO2转化率逐渐由1.34%增加到2.2%,相比于纯二氧化碳放电的转化率均有明显的提升。这主要是由于Ar原子具有较高的激发电离能级,在等离子体放电区内,氩原子被激发或电离,随着氩气比例增加,将增加CO2电子碰撞解离的概率,从而提高CO2转化率。CO2转化的实现,将有利于O、·OH、H2O2、O3、1O2等活性物质的生成(见式(4)-(11))。如图4 (b)所示,为不同气体流量对CO2转化的影响(CO2:Ar=1:9),随着气体流量的不断增加,CO2转化率逐渐降低。其主要原因是受等离子体放电功率的限制,随着气体流量的不断增加,CO2气体在放电区停留时间逐渐减少,没有足够的能量使得CO2被激发或者转化,CO2就已经离开放电区[13],从而造成CO2转化率不断降低。
-
利用一级动力学方程(3)[14]对不同条件下TC降解进行模拟
式中:C代表某一时刻TC含量(mg/L);C0代表TC初始浓度;k1代表一级反应动力学常数(min−1);t代表反应时间。
-
在气体流量为300 mL/min时,考察了不同CO2/Ar比例随着放电时间对气液相等离子体降解TC的影响(TC初始浓度为10 mg/L)。由图5(a)可知,随着氩气掺比增加,TC的降解率不断提升。在等离子体处理30 min,氩气比例由20%增加到95%时,TC降解率则从64.53%提高81.17%。与此相对应,由前文图4分析可知,随着氩气比例增加,二氧化碳转化率也随之提高,CO2转化率的提高有利于活性物质如活性氧原子、羟基等的生成,从而促进TC的降解。TC降解率不断增加。如图5 (b)可知在仅改变混合气体中Ar的比例时,随着Ar比例的增加反应速率也是逐渐增加,在CO2与Ar比例分别为1:4 、1:9 、1:19的情况下,整体反应速率分别为0.03343 min−1 、0.04436 min−1、0.05344 min−1。
-
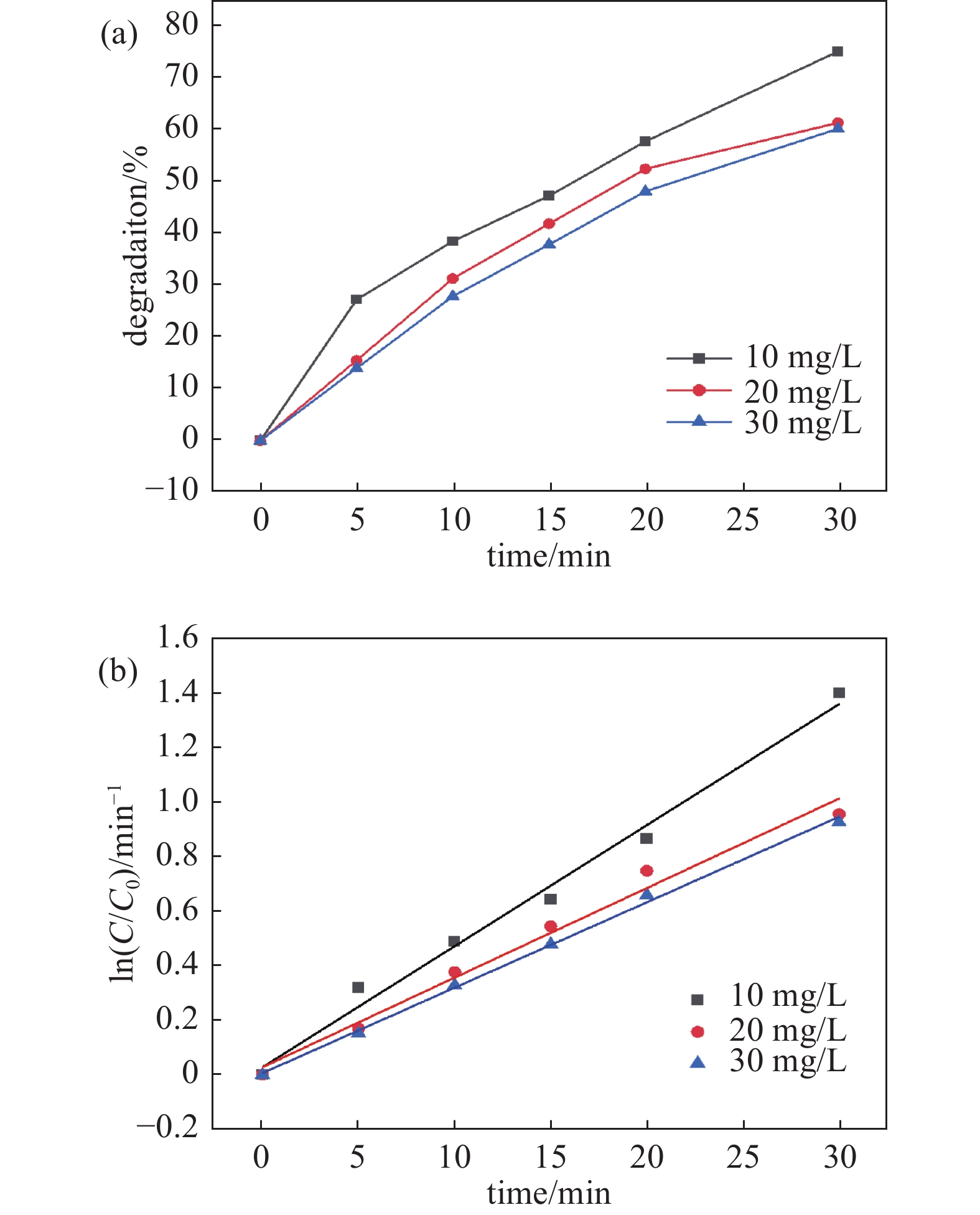
在等离子体降解过程中,污染物的不同初始浓度往往是污染物降解的一个重要因素。图6(a)显示了在气体流量为300 mL/min, CO2:Ar=1:9条件下,不同TC初始浓度其降解率随时间变化规律。当处理时间为30 min,初始浓度为10 mg/L、20 mg/L、30 mg/L时,TC降解率分别为75.35%、61.52%、60.37%,可见在10 mg/L的初始浓度条件下,TC降解效果最好。主要是由于气液相等离子体引发液相的活性物质产率、活性物质的量(·OH、H2O2等)以及与TC的反应速率是一定的,所以随着浓度的增加,单位TC可以用于反应的活性物质的量变少,且降解过程中间产物的生成也会与TC竞争产生的活性物质,使得等离子体产生的一定量活性物质未与TC反应就被消耗,最终导致TC降解率逐渐降低。如图6 (b)所示,随着浓度的升高,反应速率也是逐渐降低,也佐证了虽然浓度升高,使得单位体积内反应物质与活性物质有效反应几率增加,但活性物质的量并未发生改变,从而导致产生的活性物质不足以反应足够的TC,从而使得整体TC降解率下降。
-
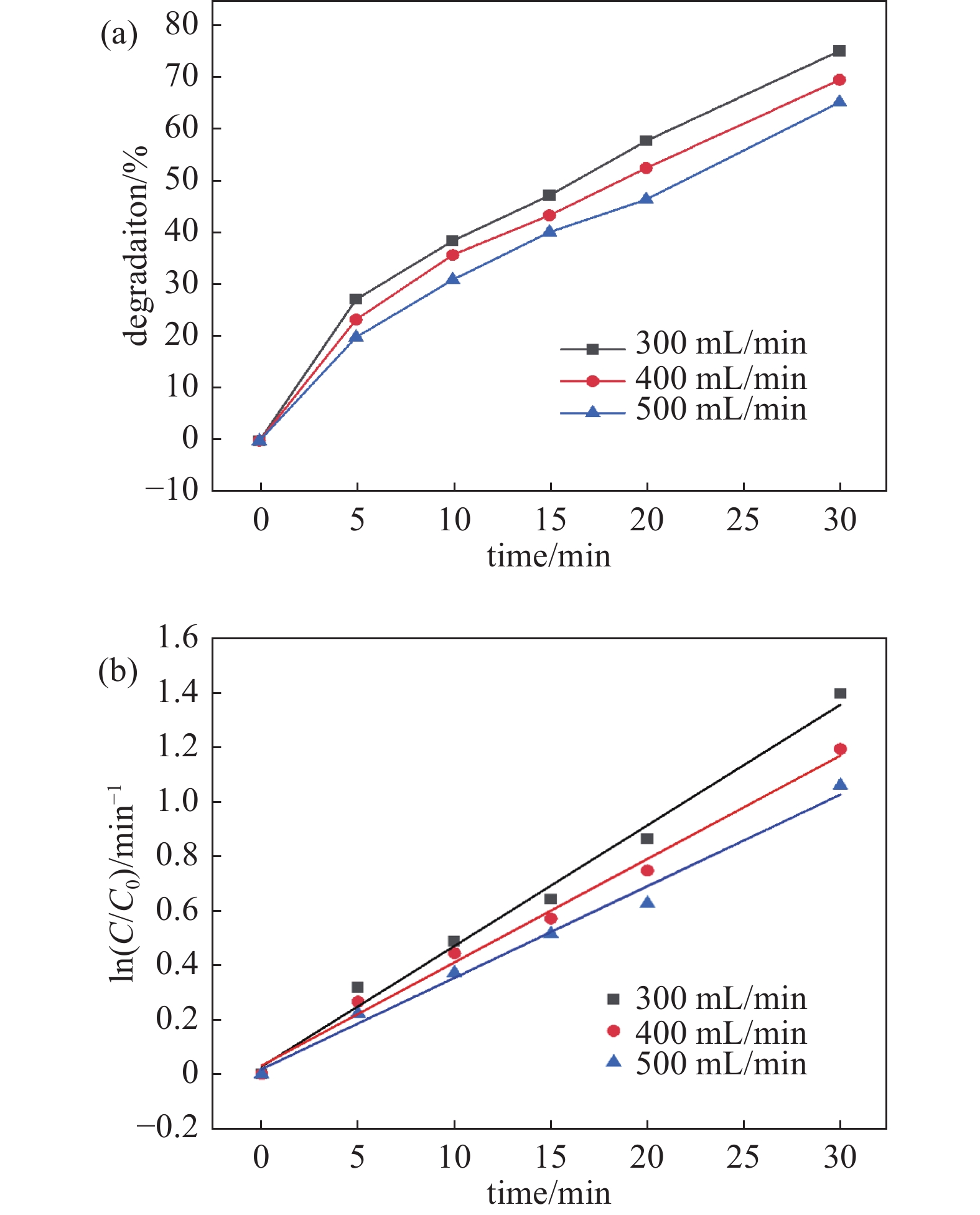
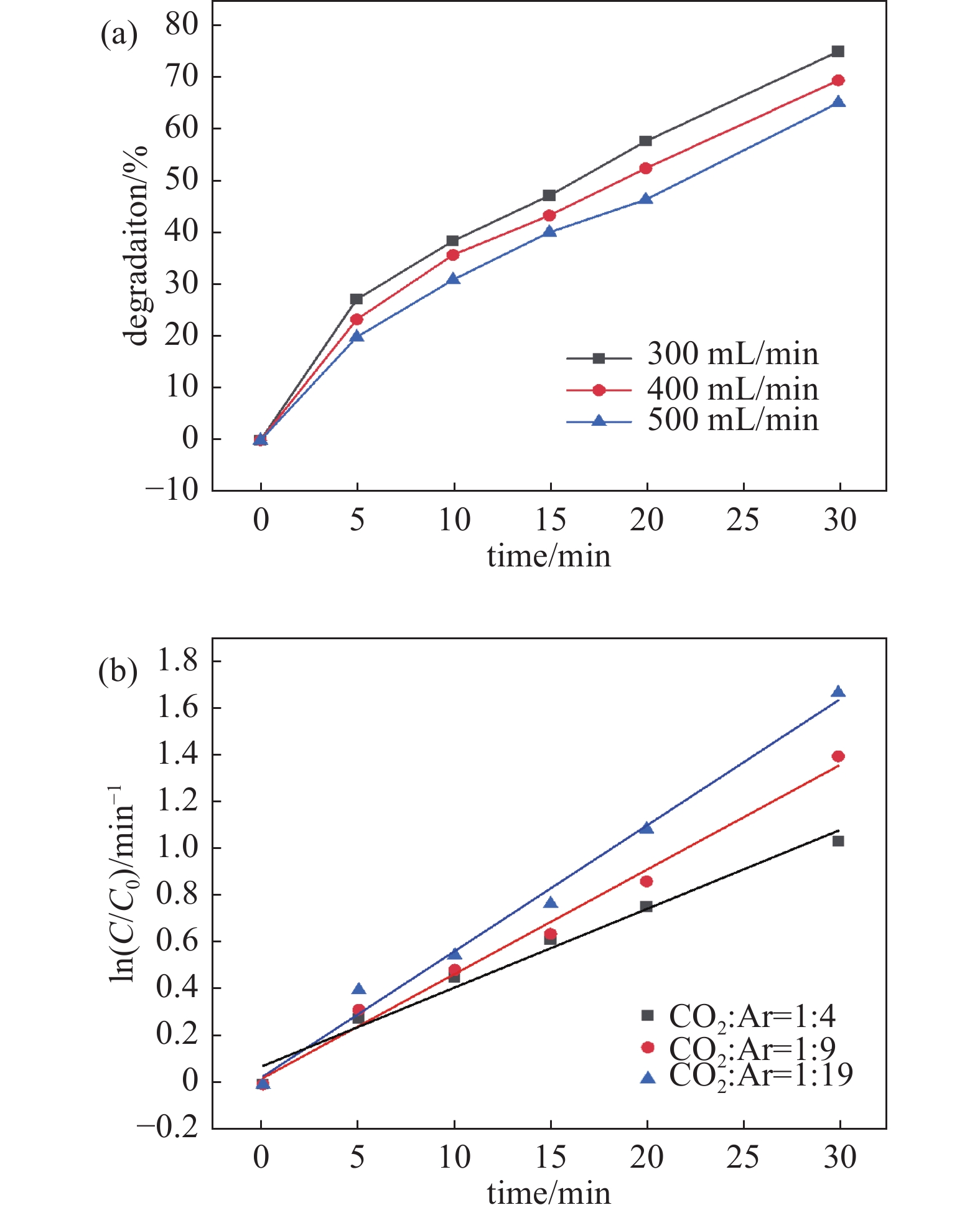
不同的气体流量会影响介质气体在放电区的停留时间,从而进一步影响产生的液相活性物质的量,而活性物质的产生量直接影响等离子体对液相污染物的降解能力,于是本文考察了气体流量这一重要影响因素对气液相等离子体降解TC的影响。图7 (a)中揭示了在初始浓度为10 mg/L、CO2:Ar=1:9条件下,不同气体流量下TC降解效率随时间变化规律。在放电时间为30 min时,气体流量为300 mL/min、400 mL/min、500 mL/min时TC的降解率分别为75.32%、69.74%、65.4%。研究发现TC降解率随气体流量增加而下降。随着气体流量的增加,气体停留时间变短,气体在放电区还未充分电离就离开放电区,从而导致产生的高能电子以及活性组分减少,另一方面随着流量的增加活性物质的停留时间也随之减少,导致其未与液相中的TC进行充分反应,从而进一步影响TC的降解率[15]。如图7(b)所示,随着气流量的增加,反应速率逐渐减少,从原来的0.04436 min−1降低到0.03365 min−1, 综合以上分析,最终选取了300 mL/min作为此次研究的气体流量条件。
-
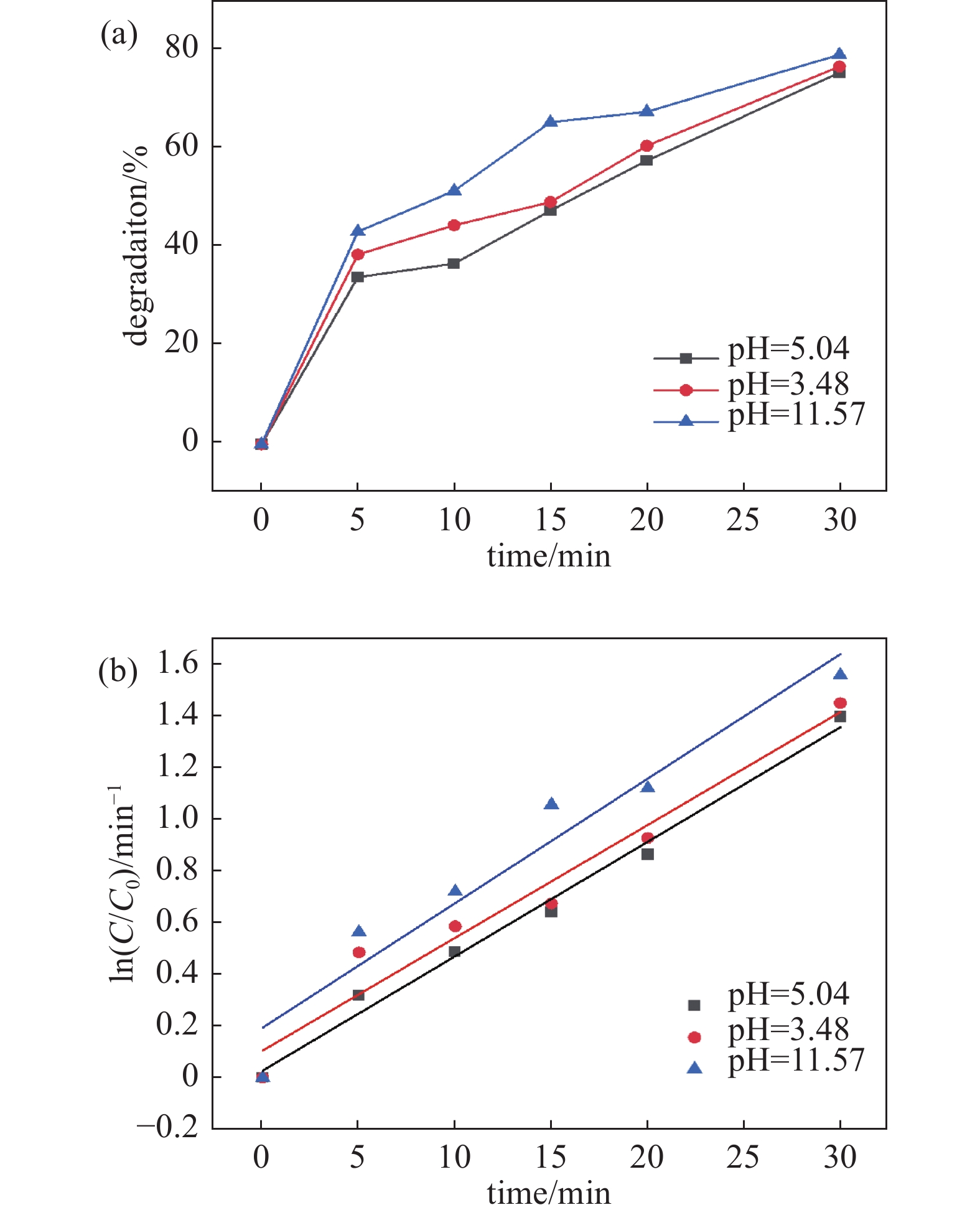
在实际应用中,抗生素废水的初始pH往往存在较大差异,所以本实验探究了不同初始pH对等离子体降解TC的影响。其结果如图8 (a)可知,碱性条件下TC降解率整体优于酸性条件。在pH为 11.57 时放电 15 min,TC 降解率可达 65.3%,而 pH 为5.04、3.48时,TC降解率则分别为49.12%、47.38%。这主要是因为一方面TC是一种两性分子,pKa值分别为3.3、7.7、9.7[16],在碱性条件下TC不稳定易失去质子形成TCH−与TC2−使之更容易被等离子体产生的活性物质降解[17];另一方面碱性条件下由于溶液中含有大量的OH−,而臭氧在碱性条件下也会被分解产生·OH,使得TC降解率增加[18]。由图8 (b) 可以看出,在不同初始pH条件下,TC反应速率有所不同。在初始pH为11.57时,TC反应速率最大(0.04824 min−1),这是因为此时溶液pH大于TC的最大pKa ,TC在水溶液里呈现出完全电离的形式存在。
-
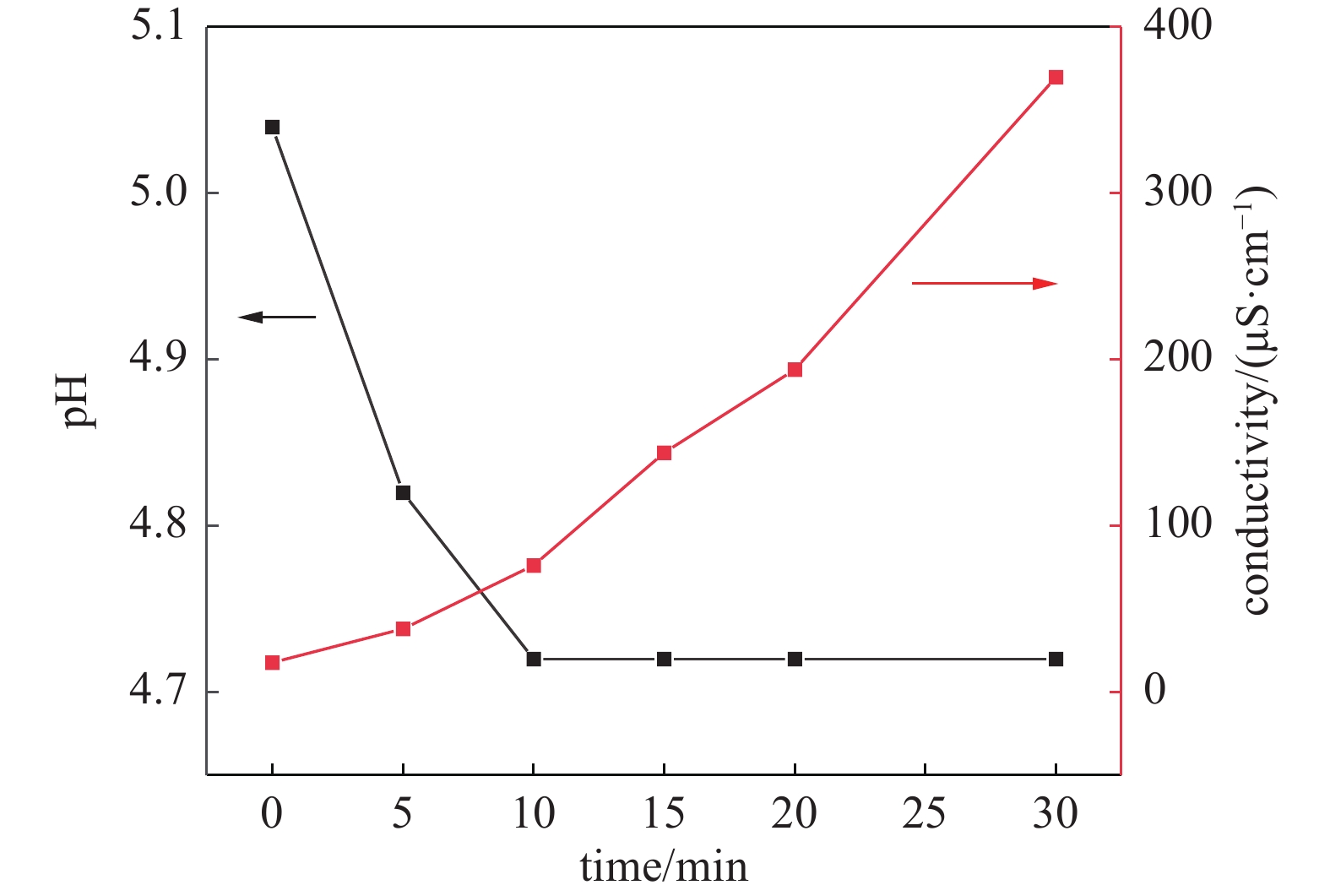
CO2/Ar气液相等离子体处理水中TC的过程中溶液中的pH及电导率的变化如图9所示。溶液中的pH在最初的10 min迅速降低,在10 min后保持稳定;而电导率则随着处理时间的延长呈现出线性增加的趋势。一方面是由于仅部分二氧化碳被分解,余下的二氧化碳溶于水会形成碳酸缓冲液;另一方面TC在被活性物质降解过程中会产生酸性的中间产物,综合考虑上述两方面作用使溶液pH一开始快速下降,但随着处理时间延长,碳酸缓冲溶液起主要作用使得整个溶液pH保持稳定。而溶液中电导率线性增加的原因主要是因为随着等离子体处理时间的增加CO32−、HCO3−等无机盐离子的不断生成。
-
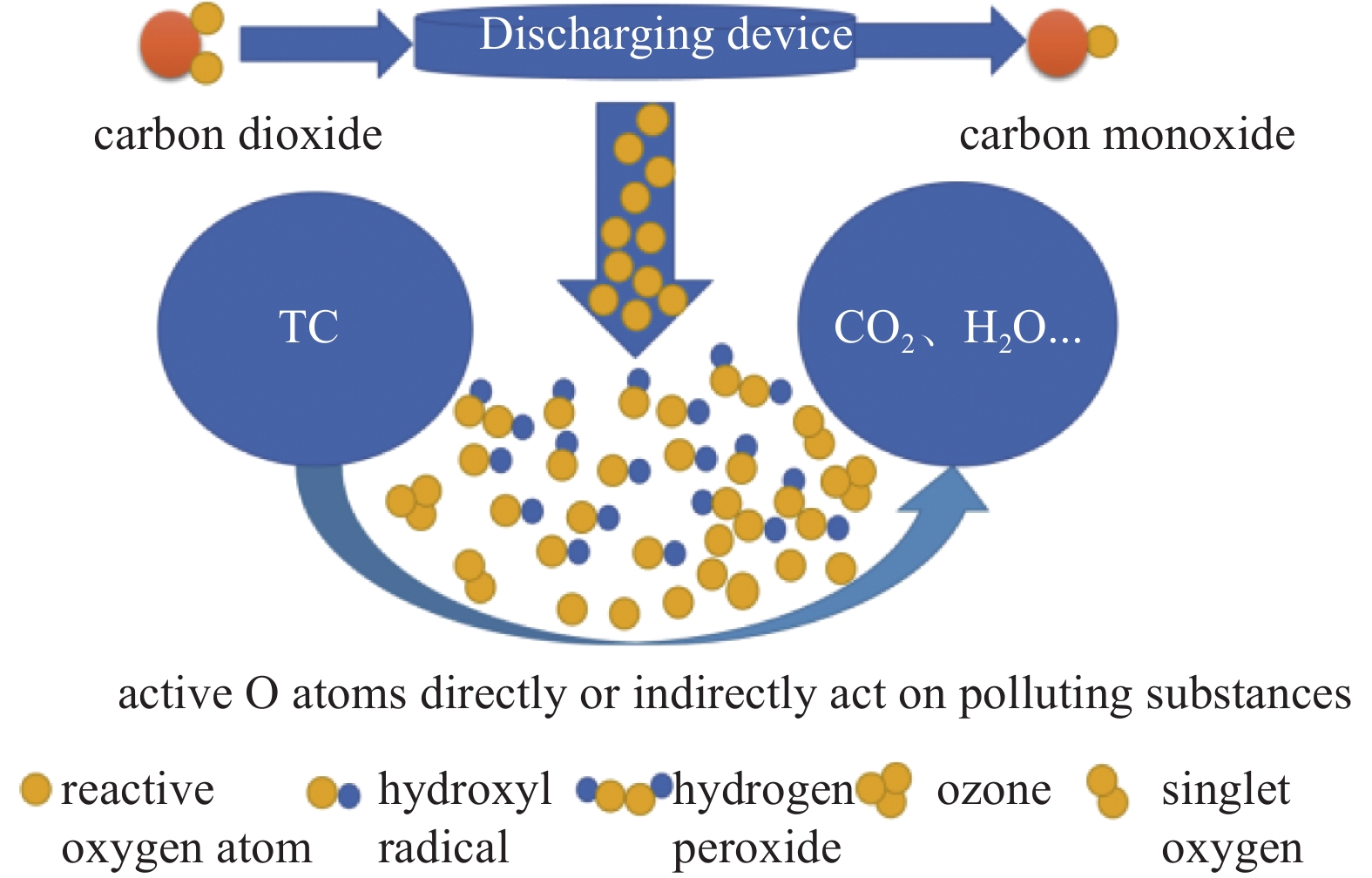
CO2/Ar 气液相等离子体放电区内,产生激发态氩原子、CO2分子、电子、离子相互作用,发生系列反应,如 CO2分解、活性氧原子产生、羟基生成、单线态氧、臭氧、双氧水生成,这些活性物质进入液相中,与溶液中的盐酸四环素反应, 达到降解目的。CO2/Ar气液等离子体作用于盐酸四环素的机理如图10 所示。近年来研究温室气体CO2分解引起了学者的广泛关注,发现CO2可以通过电子碰撞分解而产生活性氧原子,如反应式(4)和(5)所示[19-21]。
TAKAMATSU等[22]的研究了不同气氛条件下等离子体产生的各种活性物质,采用CO2当介质气体时放电时得到了相似的结论。其分解产生的活性氧原子可以后续生成短寿命物质·OH、1O2。CO2分解产生的O在气液传质的作用下可进入水体中,与水发生反应生成·OH(式(6)),另一方面等离子体放电产生的电子也会与H2O发生碰撞产生·OH,如式(11)所示[23]。·OH 作为一种短寿命的物质,因其具有高活性可迅速与溶液中TC发生反应使其降解。而·OH还会发生如式(7)的反应,进一步生成H2O2。活性O原子可以通过式(8)和式(9)生成O3、1O2。而O3会与H2O发生反应生成H2O2,如式(10)所示。
-
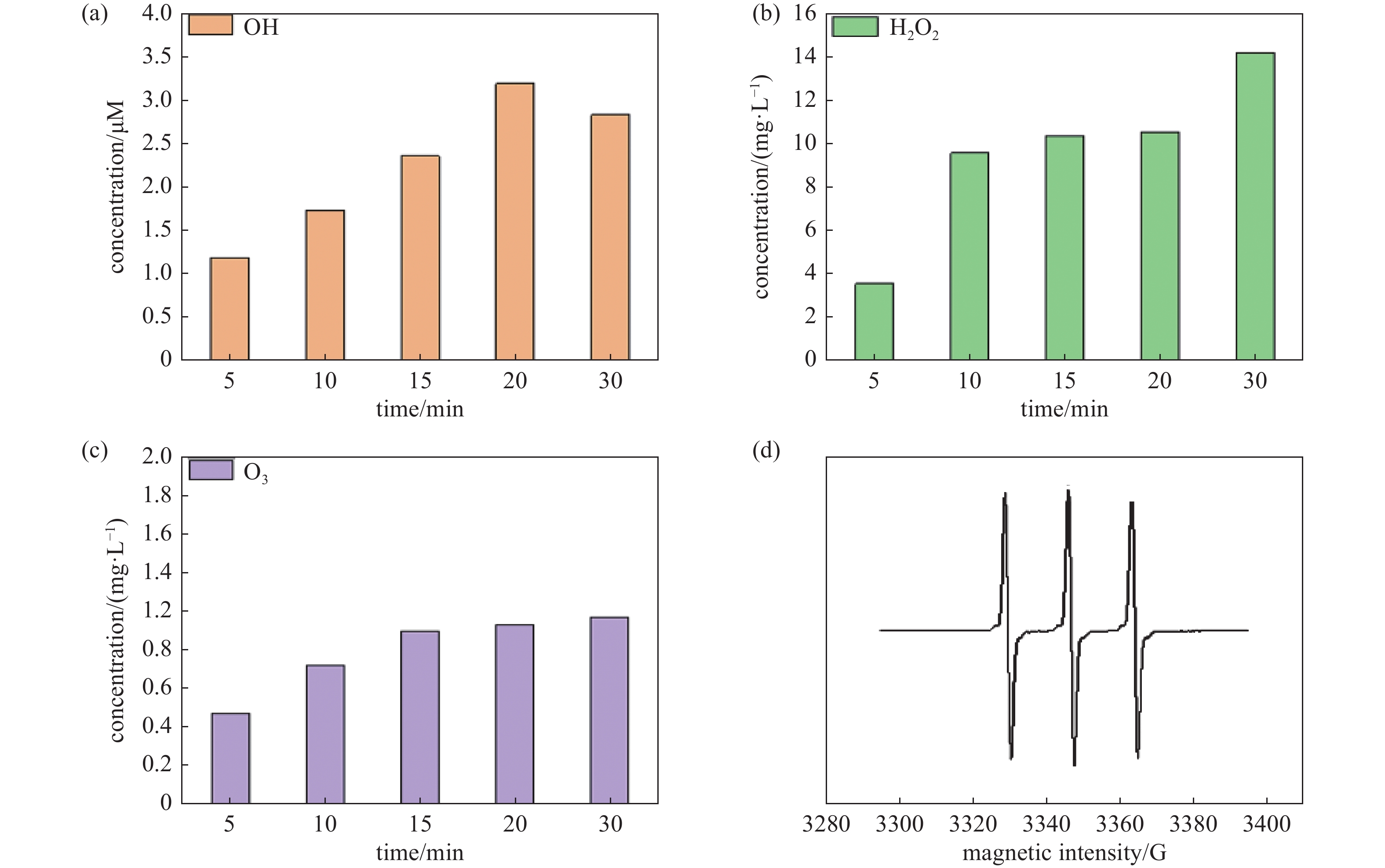
CO2/Ar等离子体与水溶液相互作用,随着CO2的分解,产生各类活性物质,在气流作用下传质到液相中,与液相中TC发生系列反应而将其降解。其中·OH、1O2属于短寿命活性物质,而H2O2、 O3属于长寿命活性物质。本实验对气液相等离子产生的·OH、H2O2、O3进行了定量的测定,对1O2进行了定性的测定。如图11(a)所示,随着等离子体放电的进行,·OH含量先增加后降低,由于·OH测量是通过探针对苯二甲酸(TA)捕获·OH形成2-羟基对苯二甲酸(HTA),随着反应的进行,TA逐渐被消耗,导致没有足够的TA对新产生的·OH进行捕获,过量的·OH或其他活性物质对产生的HTA进行分解导致·OH含量下降[5]。而H2O2、O3含量如图11(b)和(c)所示,随着放电时间增长而增加,是由于等离子体作用下CO2分解产生的活性氧原子进入水体中,有利于H2O2、O3的生成。采用TEMP对产生的1O2进行捕获形成TEMPO.,然后通过电子自旋共振(ESR)对其进行检测,如图11(d)可以观察到有1O2产生。
-
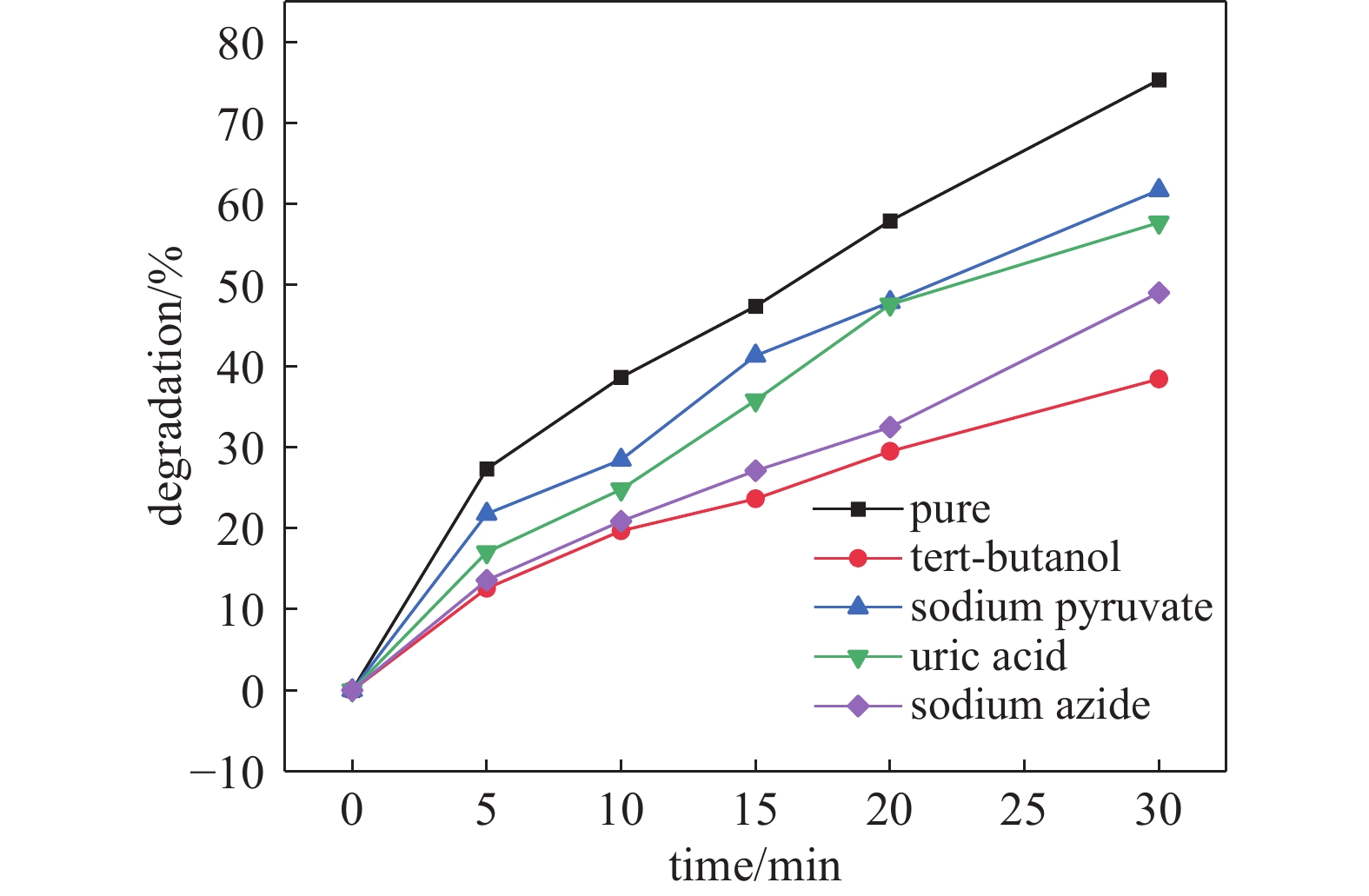
由于CO2/Ar气液相等离子体放电体系产生了不同的活性物质,为了探究在本体系中哪一种活性物质占据主导地位,通过加入不同的自由基清除剂(叔丁醇、丙酮酸钠、尿酸、叠氮化钠)以此(·OH、H2O2、O3、1O2)进行相关探究[24]。如图12所示,在等离子体处理30 min时,加入叔丁醇时,TC降解率由75.32%降低到38.41%,降低了36.91%;其次是叠氮化钠,TC降解率降低到49.07%;影响最小的是加入尿酸的情况,TC降解率仅降低到61.72%。这表明,CO2/Ar气液相放电等离子体产生的·OH为降解TC的主要活性物质。
-
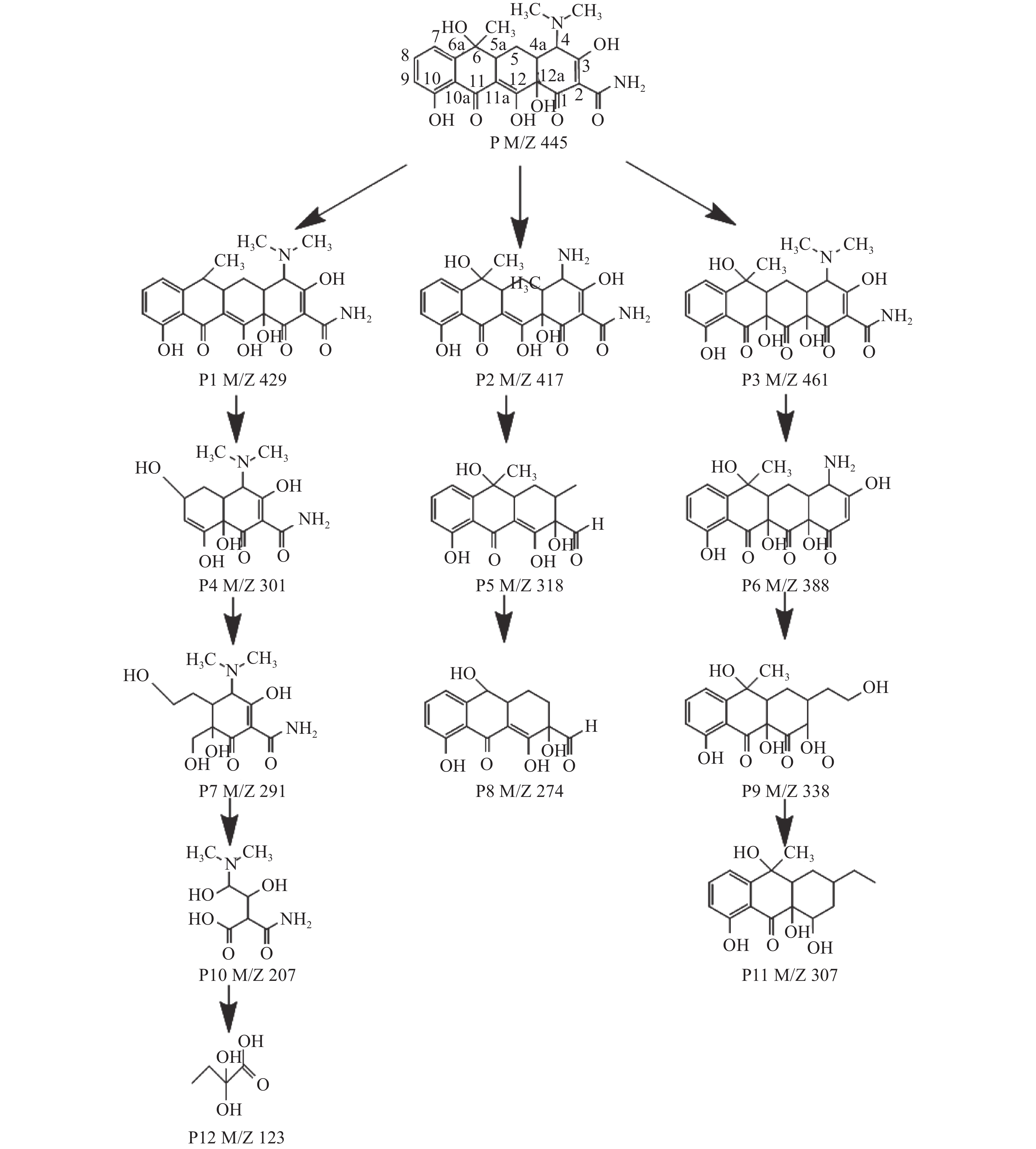
为了确定TC降解过程中产生的降解产物进而推断出其可能的降解路径,采用高效液相-质谱联用仪(LC-MS)测定等离子体处理后的TC水溶液,并对所得结果进行分析。根据物质的分子离子峰和碎片离子峰信息,推测各中间降解产物的结构,分别以P1-P12表示。在整个反应体系中,由于碳碳双键、酚基、胺基有较高的电子密度,因此这三类官能团很容易受到自由基攻击[25],TC可以通过脱水、脱甲基、羟基化等方式产生多种中间代谢产物。等离子体降解TC的三种可能降解路线如图13所示。
第一条可能的路线是P(m/z=445)发生脱水反应形成P1(m/z=429)[26-27],P1通过与等离子体产生的活性物质发生连续开环反应及OH的加成先后形成了中间产物P4(m/z=301)、P7(m/z=291)、P10(m/z=207)、P12(m/z=123),Xu等[28]在利用UVC和UVC /过硫酸盐工艺去除水中四环素的实验研究中发现与上述相似的反应机理降解路径。P12等小分子物质继而被氧化分解为CO2和H2O。
第二条可能的路线中首先是P在C4位置被1O2攻击发生脱甲基反应形成化合物P2(m/z=417)[29-31],随后P2在·OH的攻击下在C2-C3,C3-C4发生开环反应并脱去了胺基形成化合物P5 (m/z=318),紧接着P5又在·OH的攻击下发生脱甲基反应脱去C4、C6位置上的甲基形成化合物P8 (m/z=274) [32]。
第三条可能的路线为P中C11a-C12的碳碳双键较C2-C3碳碳双键电子密度更高,更容易受到·OH攻击,因此在C11a以及C12处分别形成一个羟基和一个酮基,形成了P3 (m/z=461)。Wang等以及Li等在分别利用BiOCl @ CeO2,ZnO/CeO2 @ HNTs异质结构材质高效光催化降解四环素等实验研究中也见有相似报道[33-34]。随后P3在电子攻击下发生脱甲基和酰胺基形成P6 (m/z=388) [35],P6在·OH攻击下发生脱氨基和开环反应形成P9(m/z=338),P9在·OH攻击下发生去羟基反应形成化合物P11 (m/z=307) [36],随后这些中间产物进一步被氧化产生CO2、H2O和其他无机离子。
-
本文考察了CO2/Ar气液相等离子体物理和化学特性,分析了CO2/Ar气液相反应体系中,激发态原子、CO2分子、电子、离子产生及气液通道中引发活性物质相关反应过程。如CO2分解、活性氧原子产生、羟基生成、单线态氧、臭氧和双氧水生成,这些活性物质进入液相中,与溶液中的TC反应,达到降解目的。CO2/Ar气液相等离子体在CO2与Ar比例为1:9,总气体流量为300 mL/min条件下降解了75.32%,实现了利用温室气体CO2来降解液相污染物TC,为后续CO2利用、水污染处理提供了一个新的思路。
分析了不同参数条件下,CO2/Ar气液相等离子降解TC的降解率。气体流量300 mL/min,TC降解率随着CO2分解率增加而增加,这与CO2分解、O原子、·OH等活性物质的生成有关。考察了不同初始浓度TC和不同气体流量,气液相等离子体对TC降解的影响。分析不同初始pH条件下对TC降解的影响时,碱性条件下降解效果最好,其主要原因是由于,碱性条件下TC不稳定失去质子形成TCH−与TC2−,使之更易被等离子体产生的活性物质降解;同时臭氧在碱性条件下也会被分解产生·OH,使得TC降解增加。
研究和分析了CO2/Ar气液相等离子体产生液相活性物质(如短寿命活性物质·OH、1O2、长寿命物质H2O2、O3等)的生成规律。对·OH、H2O2、O3进行了定量分析,对1O2进行了定性分析。通过加入不同淬灭剂的方式,研究了不同活性物质在降解TC中的作用,研究发现·OH、1O2为主的活性物质对TC降解影响较大,而臭氧、过氧化氢对其影响相对较小最小。最终推测了可能的降解途径。
CO2/Ar气液相等离子体处理盐酸四环素的研究
The Treatment of Tetracycline Hydrochloride by CO2/Ar Gas-Liquid Phase Plasma
-
摘要: 研究采用温室气体、氩气(CO2/Ar)作为载气,产生气液相等离子体处理水中的盐酸四环素。研究了CO2/Ar气液相等离子体CO2分解、活性物质产生(如O、·OH、1O2、H2O2、O3)及不同参数条件下对盐酸四环素的降解机理。气相方面考察了CO2/Ar比例、气体流量对CO2转化的影响;液相方面考察了CO2/Ar比例、不同初始浓度、气体流量及初始pH对盐酸四环素降解的影响。结合光谱诊断、液相活性物质表征、相关淬灭剂,分析了不同活性物质的产生规律及对盐酸四环素降解的影响。最后检测了降解过程产生的中间产物,提出了本体系盐酸四环素降解原理及可能的降解途径。为CO2利用以及水污染治理提供一个新的思路。Abstract: In this study, greenhouse gas and argon (CO2/Ar) were used as carrier gas to produce gas-liquid plasma to treat tetracycline hydrochloride in water. The CO2 decomposition of CO2/Ar gas-liquid plasma, the production of reactive species (such as OH, 1O2, O, H2O2, O3), and the degradation mechanism of tetracycline hydrochloride under different parameters were studied. In the gas phase, the effects of CO2/Ar ratio and gas flow rate on CO2 conversion were investigated. The effects of CO2/Ar ratio, different initial concentrations, gas flow rate and initial pH on the degradation of tetracycline hydrochloride were investigated in the liquid phase. Combined with the spectral diagnosis, the characterization of liquid phase reactive species, and the relevant quenching agents, the production rules of different reactive species and their effects on the degradation of tetracycline hydrochloride were analyzed. Finally, the intermediate products produced in the degradation process were detected, and the degradation principle and possible degradation pathway of tetracycline hydrochloride in this system were proposed. It provides a new idea for CO2 utilization and water pollution control.
-

-
图 11 (a)不同时间·OH质量浓度变化;(b)不同时间H2O2质量浓度变化;(c)不同时间O3质量浓度变化;(d)1O2的检测(300 mL/min,CO2:Ar=1:9)
Figure 11. (a) Change of OH mass concentration at different time, (b) change of H2O2 mass concentration at different time, (c) change of O3 mass concentration at different time, (d) detection of 1O2 (300 mL/min, CO2:Ar=1:9)
-
[1] Dong Q,Cheng Z,Yuan Z,et al. Sewerage surveillance tracking characteristics of human antibiotic emission in sewage[J]. Journal of Cleaner Production,2022,364 [2] Bongers W,Bouwmeester H,Wolf B,et al. Plasma-driven dissociation of CO2 for fuel synthesis[J]. Plasma Processes and Polymers,2017,14(6) [3] Rumbach P,Xu R,Go D B. Electrochemical production of oxalate and formate from CO2 by solvated electrons produced using an atmospheric-pressure plasma[J]. Journal of The Electrochemical Society,2016,163(10):F1157−F61 doi: 10.1149/2.0521610jes [4] Wang L,Yi Y,Guo H,et al. Atmospheric pressure and room temperature synthesis of methanol through plasma-catalytic hydrogenation of CO2[J]. ACS Catalysis,2017,8(1):90−100 [5] Shen J,Zhang H,Xu Z,et al. Preferential production of reactive species and bactericidal efficacy of gas-liquid plasma discharge[J]. Chemical Engineering Journal,2019,362:402−12 doi: 10.1016/j.cej.2019.01.018 [6] Song W,Zhang Y,Yu J,et al. Rapid removal of polyacrylamide from wastewater by plasma in the gas-liquid interface[J]. J Environ Sci (China),2019,83:1−7 doi: 10.1016/j.jes.2019.03.015 [7] Yi K,Liu D,Chen X,et al. Plasma-enhanced chemical vapor deposition of two-dimensional materials for applications[J]. Acc Chem Res,2021,54(4):1011−22 doi: 10.1021/acs.accounts.0c00757 [8] Scholtz V,Pazlarova J,Souskova H,et al. Nonthermal plasma--A tool for decontamination and disinfection[J]. Biotechnol Adv,2015,33(6 Pt 2):1108−19 [9] Fan J,Wu H,Liu R,et al. Review on the treatment of organic wastewater by discharge plasma combined with oxidants and catalysts[J]. Environmental Science and Pollution Research,2020,28(3) [10] Wang X,Mei J,Luo J,et al. Process intensification of Tetrabromobisphenol S removal with a bubble-film hybrid plasma reactor[J]. Chemical Engineering Journal,2022,427 [11] Ramakers M,Michielsen I,Aerts R,et al. Effect of argon or helium on the CO2 conversion in a dielectric barrier discharge[J]. Plasma Processes and Polymers,2015,12(8):755−63 doi: 10.1002/ppap.201400213 [12] Xu S,Whitehead J C,Martin P A. CO2 conversion in a non-thermal, barium titanate packed bed plasma reactor: The effect of dilution by Ar and N2[J]. Chemical Engineering Journal,2017,327:764−73 doi: 10.1016/j.cej.2017.06.090 [13] Mei D,Tu X. Atmospheric pressure non-thermal plasma activation of CO2 in a packed-bed dielectric barrier discharge reactor[J]. Chemphyschem,2017,18(22):3253−9 doi: 10.1002/cphc.201700752 [14] Liu X,Lv P,Yao G,et al. Microwave-assisted synthesis of selective degradation photocatalyst by surface molecular imprinting method for the degradation of tetracycline onto ClTiO2[J]. Chemical Engineering Journal,2013,217(217) [15] Huang W J,Deng,L,Jiang S,et al. High-pressure pulse discharge plasma treatment of drilling fluid wastewater[J]. Industrial Water Treatment,2018,38(06):57−60 (黄文章,邓磊,蒋姝,等. 高压脉冲放电等离子体处理钻井液废水[J]. 工业水处理,2018,38(06):57−60(in chinese) Huang W J, Deng, L, Jiang S, Wang, S F, Wang, C X, and Li L. High-pressure pulse discharge plasma treatment of drilling fluid wastewater[J] Industrial Water Treatment, 2018, 38(06): 57-60 [16] Wang Q,Li P,Zhang Z,et al. Kinetics and mechanism insights into the photodegradation of tetracycline hydrochloride and ofloxacin mixed antibiotics with the flower-like BiOCl/TiO2 heterojunction[J]. Journal of Photochemistry and Photobiology A:Chemistry,2019,378:114−24 doi: 10.1016/j.jphotochem.2019.04.028 [17] Zhang X,Wang F,Wang C,et al. Photocatalysis activation of peroxodisulfate over the supported Fe3O4 catalyst derived from MIL-88A(Fe) for efficient tetracycline hydrochloride degradation[J]. Chemical Engineering Journal,2021,426 [18] Peleg M. The chemistry of ozone in the treatment of water[J]. Water Research,1976,10(5):361−365 doi: 10.1016/0043-1354(76)90052-X [19] Wang X C,Zhang T H,Sun Y,et al. Numerical study on discharge characteristics and plasma chemistry in atmospheric CO2 discharges driven by pulsed voltages[J]. Physics of Plasmas,2022,29(2):023505 doi: 10.1063/5.0080735 [20] Kozák T,Bogaerts A. Evaluation of the energy efficiency of CO2 conversion in microwave discharges using a reaction kinetics model[J]. Plasma Sources Science and Technology,2014,24(1):015024 doi: 10.1088/0963-0252/24/1/015024 [21] Snoeckx R,Bogaerts A. Plasma technology–a novel solution for CO2 conversion?[J]. Chemical Society Reviews,2017,46(19):5805−5863 doi: 10.1039/C6CS00066E [22] Takamatsu T,Uehara K,Sasaki Y,et al. Investigation of reactive species using various gas plasmas[J]. RSC Adv,2014,4(75):39901−5 doi: 10.1039/C4RA05936K [23] Liu D X,Bruggeman P,Iza F,et al. Global model of low-temperature atmospheric-pressure He+ H2O plasmas[J]. Plasma Sources Science and Technology,2010,19(2):025018 doi: 10.1088/0963-0252/19/2/025018 [24] Rothwell J G,Alam D,Carter D A,et al. The antimicrobial efficacy of plasma-activated water against Listeria and E. coli is modulated by reactor design and water composition[J]. J Appl Microbiol,2022,132(4):2490−500 doi: 10.1111/jam.15429 [25] Wang J,Zhi D,Zhou H,et al. Evaluating tetracycline degradation pathway and intermediate toxicity during the electrochemical oxidation over a Ti/Ti(4)O(7) anode[J]. Water Res,2018,137:324−34 doi: 10.1016/j.watres.2018.03.030 [26] Zhang X W,Wang F,Wang C C,et al. Photocatalysis activation of peroxodisulfate over the supported Fe3O4 catalyst derived from MIL-88A (Fe) for efficient tetracycline hydrochloride degradation[J]. Chemical Engineering Journal,2021,426:131927 doi: 10.1016/j.cej.2021.131927 [27] Li H,Sun S,Ji H,et al. Enhanced activation of molecular oxygen and degradation of tetracycline over Cu-S4 atomic clusters[J]. Applied Catalysis B:Environmental,2020,272:118966 doi: 10.1016/j.apcatb.2020.118966 [28] Xu M,Deng J,Cai A,et al. Comparison of UVC and UVC/persulfate processes for tetracycline removal in water[J]. Chemical Engineering Journal,2020,384:123320 doi: 10.1016/j.cej.2019.123320 [29] Guo D,Liu Y,Ji H,et al. Silicate-enhanced heterogeneous flow-through electro-Fenton system using iron oxides under nanoconfinement[J]. Environmental Science & Technology,2021,55(6):4045−4053 [30] Chen Y,Yin R,Zeng L,et al. Insight into the effects of hydroxyl groups on the rates and pathways of tetracycline antibiotics degradation in the carbon black activated peroxydisulfate oxidation process[J]. Journal of Hazardous Materials,2021,412:125256 doi: 10.1016/j.jhazmat.2021.125256 [31] Kubiak A,Bielan Z,Kubacka M,et al. Microwave-assisted synthesis of a TiO2-CuO heterojunction with enhanced photocatalytic activity against tetracycline[J]. Applied Surface Science,2020,520:146344.(417) [32] Hu Y,Chen D,Zhang R,et al. Singlet oxygen-dominated activation of peroxymonosulfate by passion fruit shell derived biochar for catalytic degradation of tetracycline through a non-radical oxidation pathway[J]. Journal of Hazardous Materials,2021,419:126495 doi: 10.1016/j.jhazmat.2021.126495 [33] Wang H,Liao B,Lu T,et al. Enhanced visible-light photocatalytic degradation of tetracycline by a novel hollow BiOCl@CeO2 heterostructured microspheres: Structural characterization and reaction mechanism[J]. Journal of hazardous materials,2020,385:121552 doi: 10.1016/j.jhazmat.2019.121552 [34] Ye Z,Li J,Zhou M,et al. Well-dispersed nebula-like ZnO/CeO2@ HNTs heterostructure for efficient photocatalytic degradation of tetracycline[J]. Chemical Engineering Journal,2016,304:917−933 doi: 10.1016/j.cej.2016.07.014 [35] Li S,Wang C,Liu Y,et al. Photocatalytic degradation of tetracycline antibiotic by a novel Bi2Sn2O7/Bi2MoO6 S-scheme heterojunction: performance, mechanism insight and toxicity assessment[J]. Chemical Engineering Journal,2022,429:132519 doi: 10.1016/j.cej.2021.132519 [36] Li S,Wang C,Liu Y,et al. Photocatalytic degradation of antibiotics using a novel Ag/Ag2S/Bi2MoO6 plasmonic pnheterojunction photocatalyst: Mineralization activity, degradation pathways and boosted charge separation mechanism[J]. Chemical Engineering Journal,2021,415:128991 doi: 10.1016/j.cej.2021.128991 -


 首页
首页 登录
登录 注册
注册
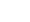


 下载:
下载: