-
表面增强拉曼光谱(surface enhanced Raman spectroscopy, SERS)能够提供丰富的分子结构信息, 可在单分子水平实现超灵敏、无损、快速检测, 已广泛应用于物理、化学、生物医药、环境科学、材料科学等领域[1–4]. 目前普遍认可的拉曼信号增强现象主要归功于局域表面等离激元共振效应, 即SERS的电磁场增强机制. 具体来说, 当激发光波长与金属导带电子的共振频率相匹配时, 可在金属纳米结构表面激发表面等离激元共振, 基于共振效应, 金属纳米结构在间隙区域会产生强局域电磁场, 可极大增强处于局域场中分子的拉曼信号, 增强因子可达109以上[5,6]. 然而, 电磁机制未能完全阐明不同振动模式之间增强幅度的差异, 因此, 研究人员提出基于分子与基底之间由电荷转移引起的化学增强机制理论[7]. 电荷转移可改变分子的电子密度分布, 从而导致更大的极化率, 理论上对拉曼信号的增强可达103以上.
在目前已报道的众多SERS基底类型中, 金(Au)、银(Ag)、铜(Cu)等贵金属纳米结构SERS基底在灵敏度方面有巨大优势. 然而, 纯金属SERS基底仍存在信号重现性低, 背景荧光强, 普适性差等问题, 研究人员利用非金属纳米材料性质稳定、结构可调、生物相容性好等特点[8,9], 制备了多类型非金属/金属复合结构作为SERS基底, 如Au/Ag-石墨烯[10,11]、Ag/ZnO[12]、Au/Ag-TiO2[13,14]、Au/ Ag-MoS2[15,16]等. 研究证明非金属/金属复合结构 SERS基底在传感领域具备较大的应用潜力[17–23]. 然而, 复合结构中的非金属纳米材料通常对总体拉曼增强的作用较小.
二硫化钼(MoS2)因其独特的电子、光学和机械性能而受到广泛关注, MoS2具备优异的分子吸附和荧光猝灭能力, 同时其带隙可调特性和酸碱稳定性使其在SERS领域的应用具有显著优势[23–25]. 单纯MoS2薄膜的SERS增强因子相对较小, 为了拓展其应用潜力, 研究人员将MoS2与金属纳米结构复合进一步调控其SERS性能. 例如, Yuan等[23]制备一种金纳米线(Au NWs)复合MoS2纳米片的杂化结构, SERS增强因子达到107, 是单纯Au NPs的104倍. Yu等[24]在双层MoS2纳米片上制备双取向银纳米线(Ag NWs), 与单纯Ag NWs基底相比, 基于Ag NWs-MoS2界面热点的倏逝电场, 实现了对R6G SERS信号的进一步增强. Zhai等[25]提出一种金纳米盘阵列和单层MoS2构成复合结构SERS基底, 通过电磁增强和化学增强的协同作用, 实现了对水产品中抗菌剂残留的检测[26]. 然而, 上述MoS2皆为二维薄膜形式, 适当增大材料表面粗糙度或引入不同形态的纳米结构可有效增强光吸收和分子的吸附, 进一步提升检测灵敏度.
本工作在钼箔上直接生长了大面积、竖直排列的MoS2纳米片, 并将其与银纳米颗粒(Ag NPs)复合, 制备MoS2/Ag基底, 用于SERS检测. 竖直排列的MoS2纳米片可有效增强基底对分子的吸附和光吸收, 提升电磁和化学双增强机制. 实验结果表明, MoS2/Ag基底表现出优异的SERS性能, 其对R6G分子的检测极限达到了10–12 mol/L, 接近单分子检测水平, 增强因子约为1.08×109. 同时该基底在超低浓度下对分子表现出优异的信号重现性, 最终实现了对水产品中抗菌剂残留的超灵敏检测.
-
本文所用材料有钼箔(Mo, 99.98%)、去离子水、盐酸(HCl, 99.7%)、丙酮(CH3COCH3, 99.7%)、乙醇(C2H6O, 99.8%)、硫脲 (CH4N2S, 99.0%)、罗丹明6G (Rhodamine 6G, R6G).
-
图1为SERS基底的制备流程示意图. 先利用水热法在钼箔上直接生长竖直MoS2纳米片, 具体步骤如下: 将钼箔切成1.5 cm×3.0 cm大小的片; 将盐酸加入去离子水中, 稀释浓度至1 mol/L; 依次将钼箔在盐酸(1 mol/L)、丙酮、乙醇和去离子水中超声清洗10 min, 然后风干; 将1.6 g硫脲(CH4N2S) 溶解在40 mL去离子水中, 搅拌0.5 h, 转移至容量为50 mL的反应釜中, 并将清洗过的钼箔浸入其中; 其后将反应釜加热至200 ℃并保持24 h, 待冷却后收集产物, 依次利用去离子水和乙醇清洗, 烘干后即可得到竖直排列的MoS2纳米片样品. 为进一步优化, 在氩气(Ar)环境中300 ℃下对样品进一步退火1.5 h, 得到退火后MoS2纳米片. 生长完成的样品使用0.1 Å/s的速率, 通过控制时间, 在MoS2纳米片表面蒸镀不同厚度的Ag膜, 即可得到MoS2/Ag SERS基底(annealed MoS2/Ag). 作为对照, 将未经退火处理的MoS2纳米片在相同条件下蒸镀上了同样厚度的Ag.
-
利用扫描电子显微镜(scanning electron microscope, SEM, ZEISS, Gemini Sigma 500)对制备的样品进行结构表征; 使用能量色散X射线仪(energy dispersive spectrometer, EDS, ZEISS, Gemini Sigma 500)测试样品元素的分布; 利用X射线光电子能谱仪(X-ray photo electron spectroscopy, XPS, 美国赛默飞, Nexsa G2)对样品进行分析; 使用紫外-可见-近红外分光光度计(Shimadzu, SolidSpec-3700 i DUV)在室温下测得样品的反射光谱; 使用拉曼光谱仪(Horiba, HR Evolution800)记录50倍物镜下的SERS谱, 激发光波长为 532 nm, 仪器激光功率为0.48 mW, 光栅600 gr/mm.
-
图2(a), (b) 为不同放大倍数下退火后大面积竖直MoS2纳米片的SEM图, 超薄结构的MoS2纳米片直接竖直生长在钼箔上, 其形貌在微米级别上表现出良好的均匀性, 这可为均匀、高重现SERS信号的采集提供便利条件. 图2(c) 所示为未经退火处理的MoS2纳米片形貌, 经过退火处理的样品与未经退火处理的样品相比其形貌基本相同. 图2(d) 为经过退火处理后MoS2/Ag SERS基底的SEM图, 对应的Ag膜厚度为25 nm, 可以观察到基底形貌表现出明显的不同, Ag膜将MoS2纳米片均匀覆盖, 同时在纳米片边缘处形成许多团聚的Ag NPs. 图2(e), (f) 展示了退火后MoS2基底的能量色散X射线谱(EDS), Mo元素和S元素分布的高度一致证明MoS2的成功合成.
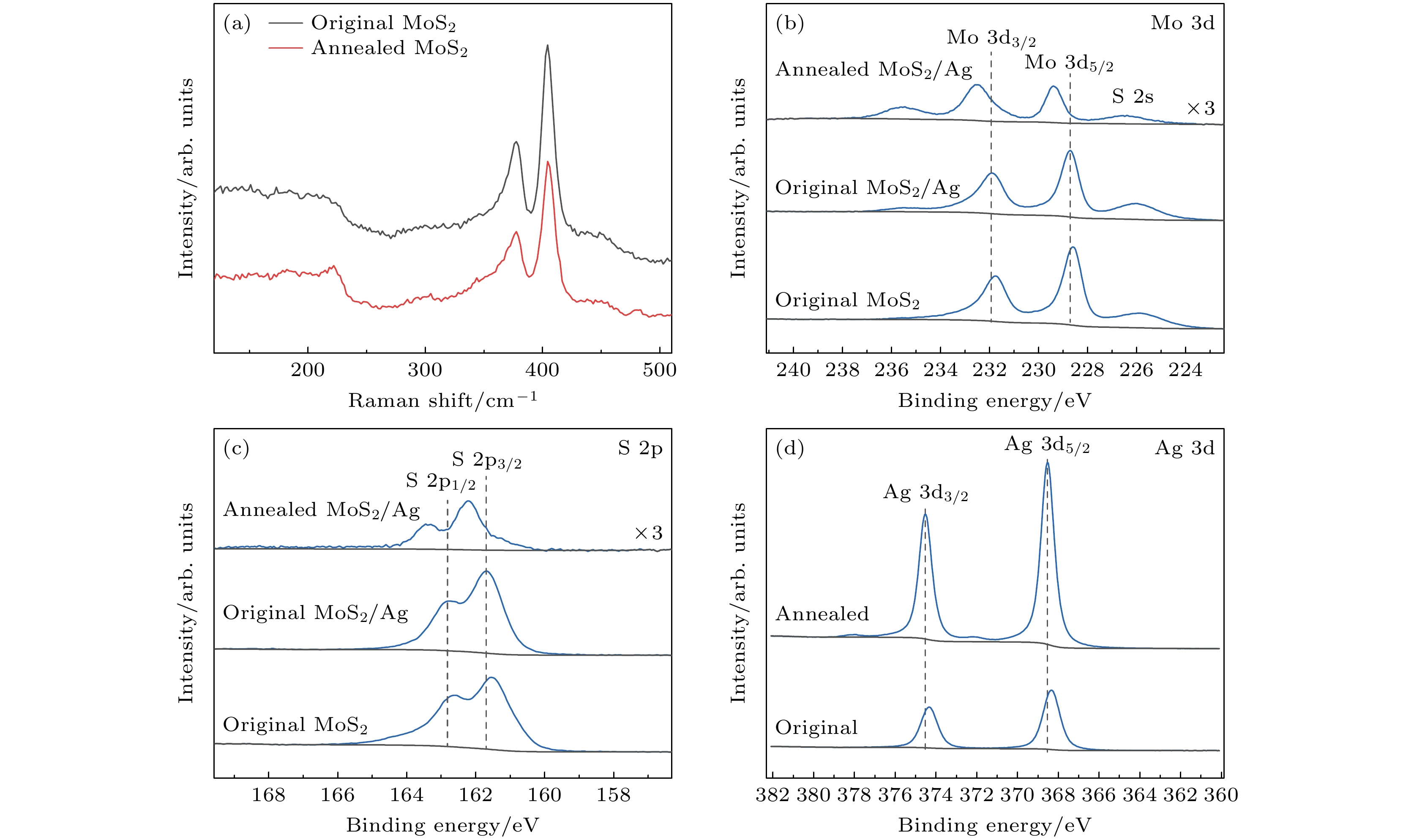
图3(a) 所示为退火前后MoS2纳米片的拉曼光谱, 进一步证明MoS2的顺利合成. 在377和404 cm–1处观察到两个不同的振动带, 分别归因于MoS2的
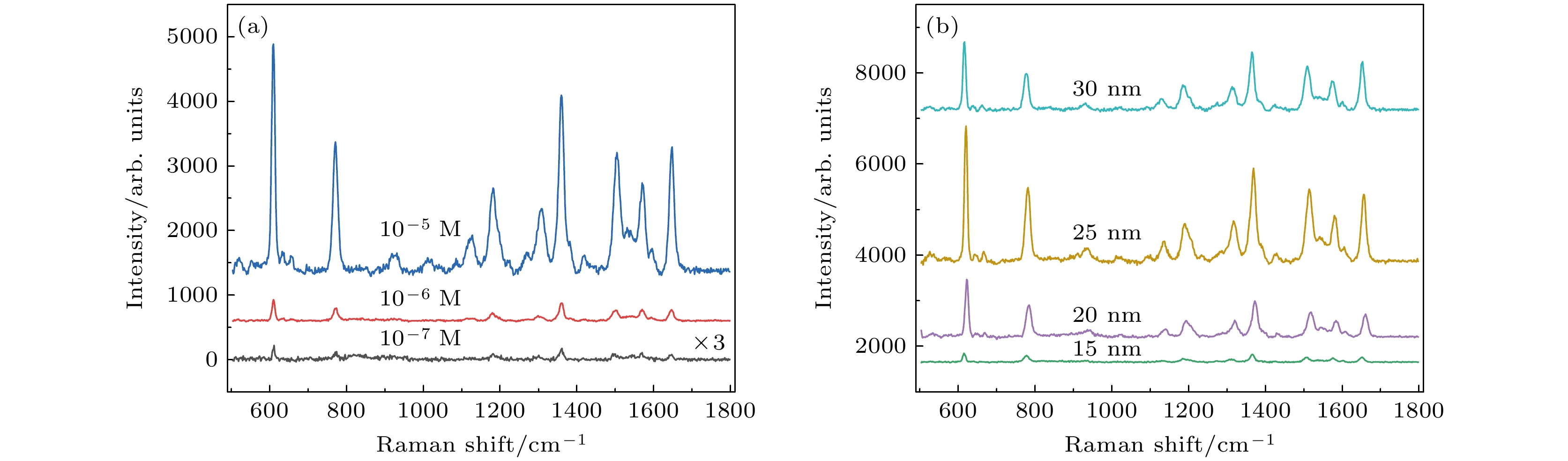
$ {\text{E}}_{{\text{2g}}}^{1} $ (面内)和A1g (面外)振动, 两个特征峰之间的波数差可用于判断MoS2的层数, 在本工作中合成的MoS2纳米片超过了4层[26,27]. 然而, 从拉曼光谱角度并不能看出退火过程对材料的影响. 进一步通过X射线光电子能谱(XPS)对两种样品进行表征. XPS光谱结合能由C 1s - 284.8 eV标定. 图3(b), (c)分别比较了退火前后样品Mo和S元素的XPS光谱变化. 图3(b)中退火后MoS2/Ag的Mo 3d在229.4和232.5 eV出现两个峰, 分别对应Mo 3d5/2和Mo 3d3/2, 与未复合Ag的MoS2基底相比, 结合能上移了约0.3 eV; 而未经退火MoS2在蒸镀Ag后Mo 3d峰位发生了约0.1 eV的蓝移. 同样, 在图3(c) 所示的S 2p峰中观察到结合能的上移. 这些结果表明, 在MoS2/Ag基底中, 电子从MoS2向Ag转移, 而且经过退火处理后更多的电子从MoS2转移到Ag[28,29], MoS2与Ag之间的相互作用变强, 这有利于SERS的化学增强.如图4所示, 首先对MoS2和未经退火MoS2/Ag基底的SERS性能进行探究. 选用R6G为探针分子, 图4(a)所示为不同浓度R6G分子在竖直MoS2 纳米片基底上的SERS光谱, 可以清楚地观察到分子的特征峰. 例如, 613 cm–1处特征峰归因于芳香族C—C—C弯曲, 774和1183 cm–1处的振动模式对应于芳香族C—H弯曲, 1572 cm–1为C=C拉伸, 1311, 1361, 1507和1648 cm–1处的峰为C—C拉伸[30]. MoS2纳米片SERS基底对R6G分子的检测极限为10–7 mol/L. 图4(b) 为浓度为10–6 mol/L的R6G在蒸镀不同厚度Ag后未经退火的MoS2基底上的SERS强度对比. 可以清楚地观察到, 随着Ag膜厚度的增大, MoS2/Ag基底SERS灵敏度随之增强. 当银膜厚度达到25 nm厚时, 基底SERS效应达到最强.
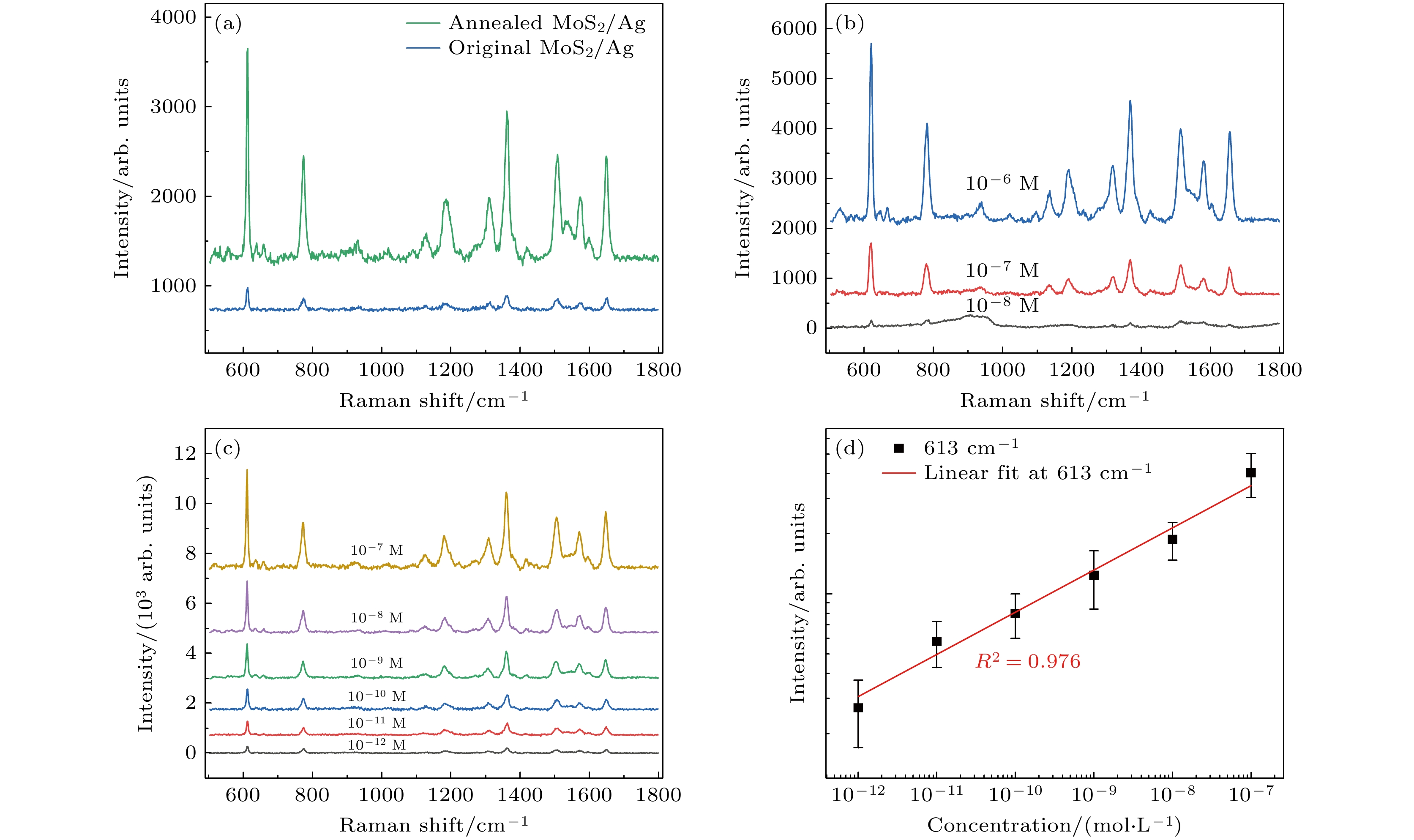
如图5(a) 所示, 对经过退火处理和未经退火处理的MoS2/Ag基底对10–5 mol/L浓度的R6G分子的测试性能进行对比. 与未经退火MoS2/Ag基底相比, R6G分子的SERS信号在经过退火处理的MoS2/Ag基底上表现出显著增强. 检测极限是评估SERS基底测试能力的另一个重要因素, 图5(b), (c)分别为未经退火和退火后MoS2/Ag基底的检测极限测试, 从图中可以看出, 未经退火MoS2/Ag基底对R6G分子的检测极限可以达到10–8 mol/L, 经退火处理的MoS2/Ag基底对R6G分子的检测极限则进一步降低到10–12 mol/L, 降低了4个数量级. 为了定量地评估SERS效应, 使用以下公式计算基底的增强因子:
其中, NSERS和Nbulk分别表示参与SERS和正常拉曼测试的探针分子数量, ISERS和Ibulk表示SERS和正常拉曼信号的强度. 计算得到, 经退火处理的MoS2/Ag基底对R6G的增强因子约为1.08×109, 远远大于未经退火处理MoS2/Ag基底的5.92×105. 最后, 如图5(d) 所示, 我们给出了吸附在MoS2/Ag基底上的R6G分子在613 cm–1处拉曼峰强度的对数与R6G分子浓度对数的线性关系, R6G分子的SERS信号强度的对数随着浓度对数的变化呈现出良好的线性关系, 拟合之后的线性系数为0.976.
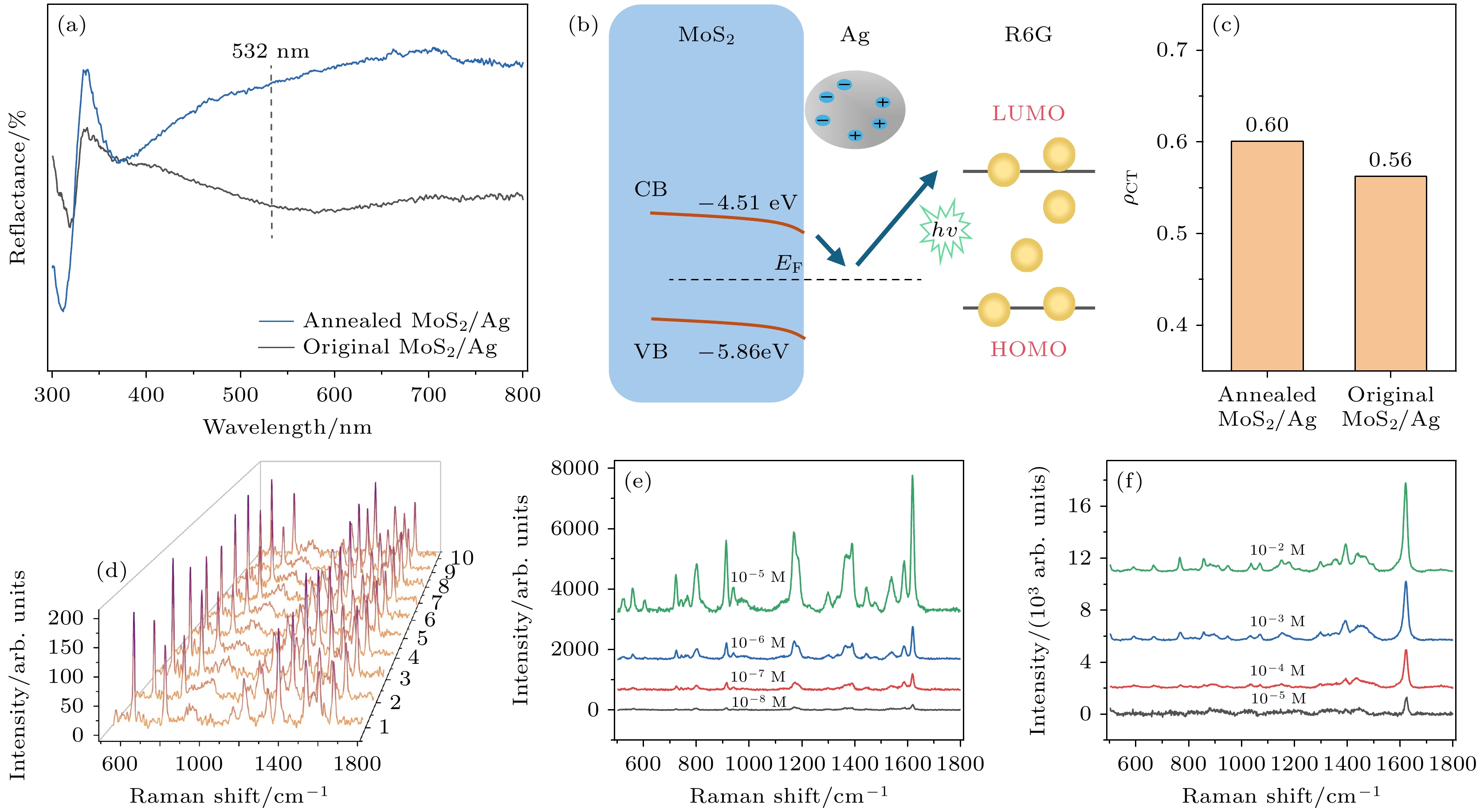
分别从电磁和化学机制角度对MoS2/Ag SERS基底的增强机理进行分析. 首先, 电磁机制方面, 对于二维MoS2薄膜, 三维竖直MoS2纳米片具有更大的比表面积, 使Ag能很好地附着, 为SERS测试提供高密度的热点区域. 图6(a) 展示了经过退火和未经退火MoS2/Ag基底的紫外-可见反射光谱, 未退火MoS2/Ag基底在400—800 nm波段表现出明显的吸收, 而经过退火处理MoS2/Ag基底的吸收波段在300—450 nm. 我们用于SERS测试的激发光波长选择的是532 nm, 因此未退火MoS2/Ag基底表现出更强的等离激元共振, 激发更大的电磁场增强. 我们从化学机制角度进一步分析, 如图6(b)所示, MoS2和Ag具有不同的功函数, 在MoS2和Ag的交界处会形成肖特基势垒, MoS2和Ag的功函数分别在5.3 eV[31–34]和4.9 eV[35]左右, MoS2和Ag的功函数差异导致半导体能带向下弯曲, 在基态情况下, 有利于电子从MoS2向Ag转移. 而基于XPS分析的结果, 退火后MoS2与Ag之间的相互作用更强, 更多的电荷从MoS2向Ag转移. 从而在光激发下, 更多的电子将从Ag的费米能级向分子能级的跃迁, 提升化学增强贡献.
为了定量估计电荷转移对SERS的贡献, 使用如下公式计算分子k波段的相对电荷转移度(ρCT)[36,37]:
其中, Ik(CT)是光谱中电荷转移共振对SERS强度有贡献的区域内谱线(k)的强度,
$I^0 \rm (SPR)$ 是选择作为参考的完全对称波段的强度. 如果谱线(k)完全对称, 则$I^k {\rm (SPR)} = I^0 {\rm (SPR)} $ ; 如果它不是完全对称的, 则$I^k \rm (SPR) $ 是该谱线在只有表面等离子体共振对光谱有贡献的区域内的强度, 此时$I^k \rm (SPR)$ 通常很小, 在许多情况下可以假设为零. 对于R6G分子, 我们选择1361 cm–1波段的强度作为$I^0\rm (SPR) $ , 测算613 cm–1 波段的电荷转移度, 结果展示在图6(c)中. 测得退火MoS2/Ag与未退火MoS2/Ag基底的电荷转移度(ρCT)分别约为0.60和0.56.信号重现性也是一项对SERS性能评估的重要指标. 如图6(d) 所示, 在MoS2/Ag基底上采集了多组R6G (10–12 mol/L)的SERS光谱, 计算出相对标准偏差 (relative standard deviation , RSD)为15.88%, 在超低浓度下具有较高的信号再现性. 为了证明MoS2/Ag基底应用的普适性, 对在532 nm激光下的非共振增强分子结晶紫 (crystalline violet, CV)和亚甲基蓝 (methylene blue, MB)进行测试 (图6(e), (f)). 结果发现MoS2/Ag基底对CV和MB的检测限分别低至10–8 mol/L和10–5 mol/L, 同样表现出优异的检测性能.
-
本文成功制备了竖直纳米片MoS2/Ag复合结构SERS基底, 并通过对MoS2的退火处理增强了Ag与MoS2之间的相互作用, SERS效果得到极大的增强. 例如, SERS信号可以放大到10倍, 检测极限可以进一步降低4个数量级. 对其增强机理分析发现, 经退火处理的MoS2/Ag基底有利于更多的电荷从MoS2向Ag转移, 进一步增强了化学机制在SERS中的作用. 同时, 我们也对基底SERS信号的重现性和普适性进行了证明. 该研究工作有助于更好地理解分子/金属-半导体杂化体系中的SERS机理, 也会为设计制备其他金属-半导体功能性SERS基底提供重要参考.
竖直取向MoS2纳米片复合Ag基底的表面增强拉曼光谱效应及机制
Surface enhanced Raman spectroscopy effect and mechanism of vertically oriented MoS2 nanosheet composite with Ag substrate
-
摘要: 结合金属和二维纳米材料的优点, 研究人员提出了多种二维材料/金属复合结构作为表面增强拉曼光谱(SERS)基底, 然而, 复合结构中的二维纳米材料通常对总增强的作用较小. 本文提出了一种竖直排列的二硫化钼(MoS2)纳米片, 并将其与银纳米颗粒(Ag NPs)复合, 制备MoS2/Ag基底, 用于SERS检测. 竖直排列MoS2纳米片可有效提高对分子的吸附, 增强光吸收, 提升电磁和化学双机制增强. 实验结果表明, MoS2/Ag基底表现出优异的SERS性能, 其对罗丹明6G (R6G)分子的检测极限达到了10–12 mol/L, 接近单分子检测水平, 增强因子约为1.08×109. 同时该基底表现出优异的信号重现性, 最终实现了对水产品中抗菌剂残留的超灵敏检测.
-
关键词:
- 表面增强拉曼光谱 /
- 竖直排列MoS2纳米片 /
- 银纳米颗粒 /
- 电荷转移
Abstract: Surface enhanced Raman spectroscopy (SERS) can provide rich molecular structure information about ultra-sensitive, non-destructive, and rapid detection, with accuracy down to the single-molecule level. It has been widely applied to physics, chemistry, biomedicine, environmental science, materials science and other fields. Combining the advantages of metals and two-dimensional (2D) nanomaterials, various 2D metal composite structures have been proposed for SERS. However, the contribution of 2D nanomaterials in Raman enhancement is often limited. In this work, vertically aligned MoS2 nanosheet composite with silver nanoparticles (Ag NPs) is proposed for SERS detection. Large-area vertically aligned MoS2 nanosheets, which are grown directly on molybdenum (Mo) foil by using hydrothermal method, can effectively enhance molecular adsorption, light absorption, and provide dual electromagnetic and chemical enhancement. Furthermore, annealing treatment of the MoS2 nanosheets significantly improves the efficiency of charge transfer between Ag NPs and MoS2, thereby increasing the chemical contribution to SERS. The results demonstrate that the annealed MoS2/Ag substrate exhibits outstanding SERS performance, with a detection limit for R6G molecules as low as 10–12 mol/L, which is four orders of magnitude lower than that of the unannealed substrate. The enhancement factor (EF) is calculated to be approximately 1.08×109, approaching the sensitivity required for single-molecule detection. Additionally, the substrate has high signal reproducibility at low concentrations, enabling ultra-sensitive detection of pesticide residues in aquatic products. -

-
图 2 基底的SEM和EDS图 (a), (b)不同放大倍数下退火后大面积竖直MoS2 纳米片SEM图; (c)未退火MoS2 纳米片SEM图; (d)退火后MoS2/Ag SERS基底的SEM图; (e), (f) 退火后MoS2 SERS基底上Mo元素和S元素的EDS图
Figure 2. SEM and EDS images of substrates: (a), (b) SEM images of large-area vertical MoS2 nanosheets after annealing at different magnifications; (c) SEM image of MoS2 nanosheets before annealing; (d) SEM image of annealed MoS2/Ag SERS substrate; (e), (f) EDS images of Mo and S elements on MoS2 SERS substrate after annealing.
图 3 基底的拉曼光谱和XPS光谱 (a)未退火和退火后MoS2纳米片的拉曼光谱; 退火后MoS2/Ag、未退火MoS2/Ag和未退火MoS2 SERS基底的(b) Mo 3d和(c) S 2p XPS光谱; (d)未退火和退火后MoS2/Ag SERS基底的Ag 3d XPS光谱
Figure 3. Raman spectra and XPS spectra of substrates: (a) Raman spectra of MoS2 nanosheets before and after annealing; (b) Mo 3d and (c) S 2p XPS spectra of annealed MoS2/Ag, original MoS2/Ag and unannealed MoS2 SERS substrate; (d) Ag 3d XPS spectra of MoS2/Ag SERS substrate before and after annealing.
图 4 MoS2和MoS2/Ag基底的SERS性能 (a)不同浓度R6G分子在竖直MoS2纳米片基底上的SERS光谱; (b) R6G分子(10–6 mol/L)在不同厚度Ag复合未退火MoS2基底上的SERS光谱
Figure 4. SERS performance of MoS2 and MoS2/Ag substrates: (a) SERS spectra of different concentrations of R6G molecules on vertically aligned MoS2 nanosheet substrates; (b) SERS spectra of R6G molecules at a concentration of 10–6 mol/L on unannealed MoS2 substrates composite with Ag of different thicknesses.
图 5 MoS2/Ag基底的SERS性能 (a) 经过退火和未经退火MoS2/Ag基底采集R6G (10–5 mol/L)分子的SERS光谱; (b)不同浓度R6G分子在未退火MoS2/Ag基底上的SERS光谱; (c) 不同浓度R6G分子在退火后MoS2/Ag基底上的SERS光谱; (d) 双对数坐标下, 吸附在退火后MoS2/Ag基底上的R6G分子在613 cm–1处的拉曼峰强度与R6G分子浓度的关系
Figure 5. SERS performance of MoS2/Ag substrates: (a) Comparison of SERS spectra of R6G (10–5 mol/L) molecules collected on annealed and original MoS2/Ag substrates; (b) SERS spectra of R6G molecules with different concentrations on original MoS2/Ag substrate; (c) SERS spectra of R6G molecules with different concentrations on annealed MoS2/Ag substrate; (d) in double logarithmic coordinates, the relationship between the Raman peak intensity of R6G molecules adsorbed on the annealed MoS2/Ag substrate at 613 cm–1 and the concentration of R6G molecules.
图 6 基底的SERS增强机制分析和检测性能 (a)经过退火和未经退火MoS2/Ag基底的反射光谱; (b) MoS2/Ag基底电荷转移分析; (c)经过退火和未经退火MoS2/Ag基底上R6G分子的电荷转移度(ρCT); (d) R6G (10–12 mol/L)分子在退火后MoS2/Ag 基底的多个随机位置上的SERS光谱; (e)不同浓度CV分子在MoS2/Ag上的SERS光谱; (f)不同浓度MB分子在MoS2/Ag上的SERS光谱
Figure 6. Analysis of SERS enhancement mechanism and detection performance of substrates: (a) Diffuse reflectance spectra of annealed and original MoS2/Ag substrates; (b) charge transfer analysis of MoS2/Ag substrate; (c) charge transfer degree (ρCT) of R6G molecules on annealed MoS2/Ag and original MoS2/Ag substrate; (d) SERS spectra of R6G (10–12 mol/L) molecules at multiple random positions on annealed MoS2/Ag substrate; (e) SERS spectra of CV molecules with different concentrations on annealed MoS2/Ag substrate; (f) SERS spectra of MB molecules with different concentrations on annealed MoS2/Ag substrate.
-
[1] Brosseau C L, Colina A, Perales-Rondon J V, Wilson A J, Joshi P B, Ren B, Wang X 2023 Nat. Rev. Methods Primers 3 79 doi: 10.1038/s43586-023-00263-6 [2] Hu H F, Tian Y, Chen P P, Chu W G 2024 Adv. Mater. 36 2303001 doi: 10.1002/adma.202303001 [3] Peng Y S, Lin C L, Li Y Y, Gao Y, Wang J, He J, Huang Z R, Liu J J, Luo X Y, Yang Y 2022 Matter 5 694 doi: 10.1016/j.matt.2021.11.028 [4] Logan N, Cao C, Freitag S, Haughey S A, Krska R, Elliott C T 2024 Adv. Mater. 36 2309625 doi: 10.1002/adma.202309625 [5] Itoh T, Prochazka M, Dong Z C, Ji W, Yamamoto Y S, Zhang Y, Ozaki Y 2023 Chem. Rev. 123 1552 doi: 10.1021/acs.chemrev.2c00316 [6] Li L H, Jiang R T, Shan B B, Lu Y X, Zheng C, Li M 2022 Nat. Commun. 13 5249 doi: 10.1038/s41467-022-32975-w [7] Jensen L, Aikens C M, Schatz G C 2008 Chem. Soc. Rev. 37 1061 doi: 10.1039/b706023h [8] Feng E D, Zheng T T, He X X, Chen J Q, Gu Q Y, He X, Hu F H, Li J H, Tian Y 2023 Angew. Chem. Int. Ed. 62 e202309249 doi: 10.1002/anie.202309249 [9] Tang X, Fan X C, Zhou J, Wang S, Li M Z, Hou X Y, Jiang K W, Ni Z H, Zhao B, Hao Q, Qiu T 2023 Nano Lett. 23 7037 doi: 10.1021/acs.nanolett.3c01810 [10] Yang L, Kim T H, Cho H Y, Luo J, Lee J M, Chueng S T D, Hou Y N, Yin P T T, Han J Y, Kim J H, Chung B G, Choi J W, Lee K B 2021 Adv. Funct. Mater. 31 2006918 doi: 10.1002/adfm.202006918 [11] Jiang Y, Wang X C, Zhao G, Shi Y Y, Wu Y, Yang H L, Zhao F Y 2024 Water Res. 255 121444 doi: 10.1016/j.watres.2024.121444 [12] Hao N J, Liu P Z, Bachman H, Pei Z C, Zhang P R, Rufo J, Wang Z Y, Zhao S G, Huang T J 2020 ACS Nano 14 6150 doi: 10.1021/acsnano.0c02145 [13] Butmee P, Samphao A, Tumcharern G 2022 J. Hazard. Mater. 437 129344 doi: 10.1016/j.jhazmat.2022.129344 [14] Zhou L, Zhou J, Lai W, Yang X D, Meng J, Su L B, Gu C J, Jiang T, Pun E Y B, Shao L Y, Petti L, Sun X W, Jia Z H, Li Q X, Han J G, Mormile P 2020 Nat. Commun. 11 1785 doi: 10.1038/s41467-020-15484-6 [15] Pan H M, Dong Y, Gong L B, Zhai J Y, Song C Y, Ge Z L, Su Y, Zhu D, Chao J, Su S, Wang L H, Wan Y, Fan C H 2022 Biosens. Bioelectron. 215 114553 doi: 10.1016/j.bios.2022.114553 [16] Zhou P Y, Cheng S Y, Li Q, Pang Y F, Xiao R 2023 Chem. Eng. J. 471 144514 doi: 10.1016/j.cej.2023.144514 [17] Jalali M, Mata C D, Montermini L, Jeanne O, Hosseini, II, Gu Z L, Spinelli C, Lu Y, Tawil N, Guiot M C, He Z, Wachsmann-Hogiu S, Zhou R H, Petrecca K, Reisner W W, Rak J, Mahshid S 2023 ACS Nano 17 12052 doi: 10.1021/acsnano.2c09222 [18] Wang X Y, Zhang Y Q, Yu J H, Xie X, Deng R P, Min C J, Yuan X C 2022 ACS Nano 16 18621 doi: 10.1021/acsnano.2c07103 [19] Choi J H, Kim T H, El-said W A, Lee J H, Yang L T, Conley B, Choi J W, Lee K B 2020 Nano Lett. 20 7670 doi: 10.1021/acs.nanolett.0c03205 [20] Lin C L, Liang S S, Peng Y S, Long L, Li Y Y, Huang Z R, Long N V, Luo X Y, Liu J J, Li Z Y, Yang Y 2022 Nanomicro Lett. 14 75 doi: 10.1007/s40820-022-00803-x [21] Son W K, Choi Y S, Han Y W, Shin D W, Min K Y H, Shin J, Lee M J, Son H, Jeong D H, Kwak S Y 2023 Nat. Nanotechnol. 18 205 doi: 10.1038/s41565-022-01274-2 [22] Ge Y C, Yang Y, Zhu Y J, Yuan M L, Sun L B, Jiang D F, Liu X H, Zhang Q W, Zhang J Y, Wang Y 2024 Small 20 2302410 [23] Yuan H, Yu S, Kim M, Lee J E, Kang H, Jang D, Ramasamy M S, Kim D H 2022 Sens. Actuators B Chem. 371 132453 doi: 10.1016/j.snb.2022.132453 [24] Yu L L, Lu L, Zeng L H, Yan X H, Ren X F, Wu J 2021 J. Phys. Chem. C 125 1940 doi: 10.1021/acs.jpcc.0c08184 [25] Zhai Y J, Yang H, Zhang S N, Li J H, Shi K X, Jin F J 2021 J. Mater. Chem. C 9 6823 doi: 10.1039/D1TC00813G [26] Li H, Zhang Q, Yap C C R, Tay B K, Edwin T H T, Olivier A, Baillargeat D 2012 Adv. Funct. Mater. 22 1385 doi: 10.1002/adfm.201102111 [27] Niu Y, Gonzalez-Abad S, Frisenda R, Marauhn P, Drüppel M, Gant P, Schmidt R, Taghavi N S, Barcons D, Molina-Mendoza A J, de Vasconcellos S M, Bratschitsch R, De Lara D P, Rohlfing M, Castellanos-Gomez A 2018 Nanomaterials 8 725 doi: 10.3390/nano8090725 [28] Liu H Q, Yao C B, Li J, Sun W J, Jiang C H 2022 Appl. Surf. Sci. 571 151176 doi: 10.1016/j.apsusc.2021.151176 [29] Yu D H, Yu X D, Wang C H, Liu X C, Xing Y 2012 ACS Appl. Mater. Interfaces 4 2781 doi: 10.1021/am3004363 [30] Wang P, Liang O, Zhang W, Schroeder T, Xie Y H 2013 Adv. Mater. 25 4918 doi: 10.1002/adma.201300635 [31] Jones L A H, Xing Z D, Swallow J E N, Shiel H, Featherstone T J, Smiles M J, Fleck N, Thakur P K, Lee T L, Hardwick L J, Scanlon D O, Regoutz A, Veal T D, Dhanak V R 2022 J. Phys. Chem. C 126 21022 doi: 10.1021/acs.jpcc.2c05100 [32] Choi S, Shaolin Z, Yang W 2014 J. Korean Phys. Soc. 64 1550 doi: 10.3938/jkps.64.1550 [33] Dieringer J A, Wustholz K L, Masiello D J, Camden J P, Kleinman S L, Schatz G C, Van Duyne R P 2009 J. Am. Chem. Soc. 131 849 doi: 10.1021/ja8080154 [34] Kaushik A, Singh J, Soni R, Singh J P 2023 ACS Appl. Nano Mater. 6 9236 doi: 10.1021/acsanm.3c00813 [35] Giovannetti G, Khomyakov P A, Brocks G, Karpan V M, van den Brink J, Kelly P J 2008 Phys. Rev. Lett. 101 026803 doi: 10.1103/PhysRevLett.101.026803 [36] Chenal C, Birke R L, Lombardi J R 2008 ChemPhysChem 9 1617 doi: 10.1002/cphc.200800221 [37] Lombardi J R, Birke R L 2008 J. Phys. Chem. C 112 5605 doi: 10.1021/jp800167v -


 首页
首页 登录
登录 注册
注册
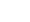


 下载:
下载: